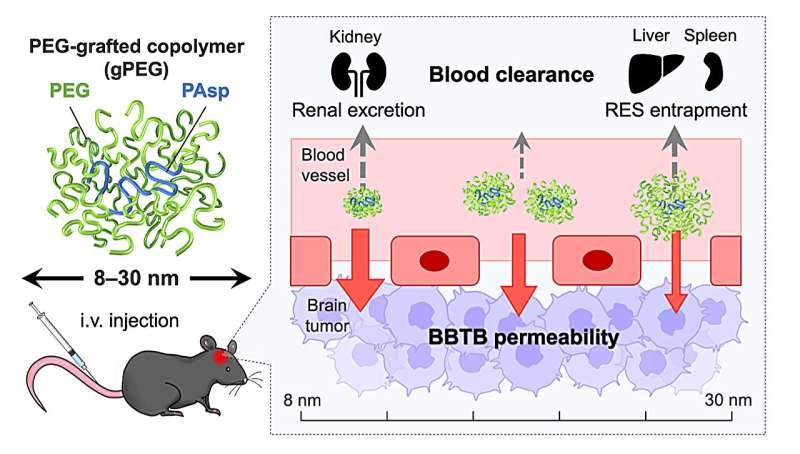
Een schematische illustratie van grootte-instelbare PEG-geënte copolymeren (gPEG’s) voor het optimaliseren van de passieve glioblastoma multiforme (GBM)-targeting. MW, moleculair gewicht; BBTB, bloed-hersentumorbarrière; iv, intraveneus; RES, reticulo-endotheliaal systeem. Credit: Kanjiro Miyata’s Lab
Momenteel is er geen effectieve behandeling voor glioblastoma multiforme (GBM), het meest voorkomende en kwaadaardige type hersentumor. Sommige antitumormiddelen met een laag moleculair gewicht worden gebruikt om de openingen tussen endotheelcellen in de BBTB (bloed-hersentumorbarrière) te doordringen, wat een karakteristieke bloedvatstructuur is en gevormd wordt door de gedeeltelijke ineenstorting van de bloed-hersenbarrière, maar ze worden snel uitgescheiden door de nieren, wat resulteert in een lage GBM-accumulatie.
Bovendien induceert hun niet-specifieke distributie in gezonde weefsels vaak ernstige bijwerkingen zoals myelosuppressie en immunosuppressie. Het is bekend dat nanomedicijnen van 30-100 nm snelle renale excretie vermijden en de efficiëntie van medicijnaccumulatie in sommige tumormodellen verhogen. Het GBM-accumulatieniveau van dergelijke nanomedicijnen blijft echter beperkt, vermoedelijk vanwege de relatief lage bloedvatpermeabiliteit in de BBTB.
Het Innovation Center of NanoMedicine (iCONM) heeft samen met de Graduate School of Engineering van de Universiteit van Tokio bekendgemaakt dat een groep onder leiding van Prof. Kanjiro Miyata, gastwetenschapper van iCONM (hoogleraar, afdeling Materiaalkunde, Universiteit van Tokio), heeft ontdekt dat de drempelwaarde voor weefselpermeabiliteit van hersentumoren in het bereik van 10-30 nm ligt. De groep heeft daarbij gebruikgemaakt van een nanoliniaal, een biocompatibel polymeer dat wordt gebruikt voor het meten van openingen in het lichaam.
Met name wanneer de grootte van de nanoruler wordt aangepast naar 10 nm, bereikt het een ongekend hoge accumulatie van hersentumoren. De verkregen resultaten hebben belangrijke richtlijnen geboden voor het ontwerp van toekomstige nanomedicijnen voor hersentumoren.
Miyata en het team bestudeerden de grootte-afhankelijke GBM-targetbaarheid met behulp van een grootte-instelbaar stealth-polymeer, een zogenaamde “polymere nanoruler”, en gerapporteerd de resultaten in het tijdschrift Bioconjugaatchemie.
Kleine gPEG’s vertoonden een efficiënte accumulatie van hersentumoren, waarbij 10 nm gPEG’s het hoogste accumulatieniveau bereikten (19 keer hoger dan dat in de normale hersenregio en 4,2 keer hoger dan dat van 30 nm gPEG’s), vermoedelijk vanwege de optimale grootte die geassocieerd wordt met een verhoogde BBTB-permeabiliteit en een verlengde bloedcirculatie.
Concluderend onderzocht deze studie het effect van nanomedicijnen op passieve GBM-targeting met poly(ethyleenglycol)-geënte copolymeren (gPEG’s) met aanpasbare grootte als polymere nanolinialen (variërend van 8,5 tot 30 nm).
Miyata zal in toekomstig werk verslag doen van de medicijnconjugatie en -optimalisatie voor de verbeterde GBM-gerichte medicijnafgifte. Over het geheel genomen biedt deze studie een bruikbaar moleculair ontwerp om GBM-gerichte nanomedicijnen te ontwikkelen voor chemotherapie, radiotherapie, fotodynamische/thermische therapie en diagnostiek.
Meer informatie:
Yukine Ishibashi et al, Grootte-afhankelijke glioblastoom-targeting door polymere nanoruler met verlengde bloedcirculatie, Bioconjugaatchemie (2024). DOI: 10.1021/acs.bioconjchem.4c00235
Informatie over het tijdschrift:
Bioconjugaatchemie
Geleverd door Innovatie Centrum voor NanoMedicine