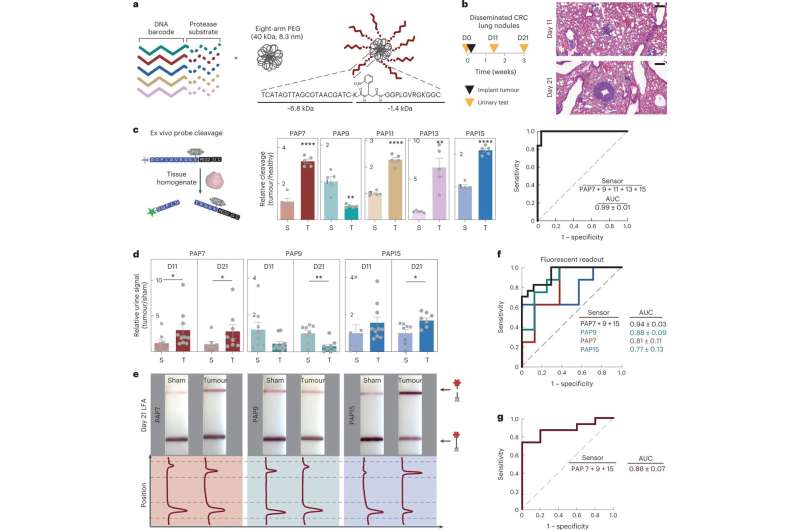
Gemultiplexte DNA-gecodeerde synthetische biomarkers voor urine voor draagbare monitoring van invasieve colorectale kanker. AGemultiplexte DNA-SUB’s bestaan uit een polymere nanodrager (achtarmige PEG) gefunctionaliseerd met protease-geactiveerde peptiden met een streepjescode met oligonucleotiden. B, Links: tijdlijn van longitudinale tumormonitoring met DNA-SUB. D, dag. Rechts: histologische longkleuring van BALB/c-muizen met CRC-longtumoren 11 dagen (bovenste) en 21 dagen (onderste) na tumor-inoculatie. Schaalbalk, 200 µm. C, Links: Schema van de fluorogene assay om peptidesubstraten te identificeren die specifiek zijn gesplitst door longweefselhomogenaten die 21 dagen na tumor-inoculatie zijn verzameld. Midden: Peptidesplitsing door CRC-dragende en gezonde longweefselhomogenaten werden gevolgd en splitsingssnelheden genormaliseerd naar gezond weefsel worden weergegeven in staafdiagrammen (N= 5 muizen per groep; gemiddelde ± sem; ongepaard tweezijdig T-test met Welch’s correctie, ****P< 0,0001 voor PAP7, **P = 0,005 voor PAP9, ****P< 0,0001 voor PAP11, **P = 0,008 voor PAP13, ****P< 0,0001 voor PAP15). Rechts: ROC-analyse van gegevens in het middelste paneel. DGepoolde DNA-SUB’s werden toegediend aan CRC-longtumordragende BALB / c-muizen (tumor, T) en met zoutoplossing geïnjecteerde controledieren (sham, S) op dag 11 of 21 na tumorinitiatie. Urinemonsters werden 1 uur na toediening van de sensor verzameld. Cas12a trans-splitsingstesten werden uitgevoerd tegen elke DNA-streepjescode en de initiële reactiesnelheden (V0) werden berekend en genormaliseerd naar die van met zoutoplossing geïnjecteerde controledieren (dag 11, n = 10 muizen per tumorgroep; dag 21, n = 8 muizen per tumorgroep; n = 8 muizen per controlegroep; gemiddelde ± sem; ongepaarde twee Mann-Whitney-test met staart, dag 11 *P= 0,0343 voor PAP7; dag 21 *P= 0,0379 voor PAP7; ongepaard tweezijdig T-test met correctie van Welch, **P= 0,0054 voor PAP9; *P= 0,0171 voor PAP15). eRepresentatieve papieren uitlezing van Cas12a-activering door verzamelde urinemonsters D. Bandintensiteiten werden gekwantificeerd met behulp van ImageJ. De bovenste piek van de curve toont de gesplitste FAM-reporter en de onderste piek toont de niet-gesplitste FAM-biotine-reporter. FROC-analyse die het vermogen aantoont van individuele of gecombineerde DNA-SUB’s om zieke muizen en gezonde controles te onderscheiden met fluorescerende uitlezing in D. GMet de papieren uitlezing erin e, gebruikte de ROC-analyse de verhouding van gekwantificeerde gesplitste reporterband ten opzichte van de overeenkomstige controleband. De stippellijn vertegenwoordigt een AUC van een willekeurige biomarkerclassificatie (0,5); de AUC van een perfecte biomarker is 1,0. Credit: Natuur Nanotechnologie(2023). DOI: 10.1038/s41565-023-01372-9
MIT-ingenieurs hebben een nieuwe nanodeeltjessensor ontworpen die een vroege diagnose van kanker mogelijk maakt met een eenvoudige urinetest. De sensoren, die veel verschillende kankerachtige eiwitten kunnen detecteren, kunnen ook worden gebruikt om het type tumor te onderscheiden of hoe deze op de behandeling reageert.
De nanodeeltjes zijn zo ontworpen dat wanneer ze een tumor tegenkomen, ze korte DNA-sequenties afwerpen die in de urine worden uitgescheiden. Door deze DNA-streepjescodes te analyseren, kunnen onderscheidende kenmerken van de tumor van een bepaalde patiënt worden onthuld. De onderzoekers hebben hun test zo ontworpen dat deze kan worden uitgevoerd met een strook papier, vergelijkbaar met een COVID-test thuis, waardoor ze hopelijk betaalbaar en toegankelijk worden voor zoveel mogelijk patiënten.
“We proberen te innoveren in een context van het beschikbaar maken van technologie voor low- en middle-resource-instellingen. Deze diagnose op papier zetten maakt deel uit van ons doel om diagnostiek te democratiseren en goedkope technologieën te creëren die u snel een antwoord kunnen geven op het punt van zorg”, zegt Sangeeta Bhatia, de John en Dorothy Wilson hoogleraar Gezondheidswetenschappen en -technologie en Elektrotechniek en Computerwetenschappen aan het MIT en lid van MIT’s Koch Institute for Integrative Cancer Research en Institute for Medical Engineering and Science.
In tests bij muizen toonden de onderzoekers aan dat ze de sensoren konden gebruiken om de activiteit te detecteren van vijf verschillende enzymen die tot expressie komen in tumoren. Ze toonden ook aan dat hun aanpak kan worden opgeschaald om ten minste 46 verschillende DNA-barcodes in één monster te onderscheiden, met behulp van een microfluïdisch apparaat om de monsters te analyseren.
Bhatia is de hoofdauteur van de krant, die vandaag verschijnt in Natuur Nanotechnologie. Liangliang Hao, een voormalig MIT-onderzoeker die nu assistent-professor biomedische technologie is aan de Boston University, is de hoofdauteur van de studie.
DNA-streepjescodes
Sinds enkele jaren ontwikkelt het laboratorium van Bhatia “synthetische biomarkers” die kunnen worden gebruikt om kanker te diagnosticeren. Dit werk bouwt voort op het concept van het detecteren van biomarkers voor kanker, zoals eiwitten of circulerende tumorcellen, in het bloedmonster van een patiënt. Deze van nature voorkomende biomarkers zijn zo zeldzaam dat het bijna onmogelijk is om ze te vinden, vooral in een vroeg stadium, maar synthetische biomarkers kunnen worden gebruikt om kleinschalige veranderingen die optreden in kleine tumoren te versterken.
In eerder werk creëerde Bhatia nanodeeltjes die de activiteit kunnen detecteren van enzymen die proteasen worden genoemd en die kankercellen helpen te ontsnappen aan hun oorspronkelijke locaties of zich in nieuwe te nestelen door eiwitten van de extracellulaire matrix te doorsnijden. De nanodeeltjes zijn gecoat met peptiden die worden gesplitst door verschillende proteasen, en zodra deze peptiden in de bloedbaan zijn vrijgegeven, kunnen ze worden geconcentreerd en gemakkelijker worden gedetecteerd in een urinemonster.
De oorspronkelijke peptide-biomarkers zijn ontworpen om te worden gedetecteerd op basis van kleine gemanipuleerde variaties in hun massa, met behulp van een massaspectrometer. Dit soort apparatuur is misschien niet beschikbaar in omgevingen met weinig middelen, dus gingen de onderzoekers op zoek naar sensoren die gemakkelijker en goedkoper konden worden geanalyseerd, met behulp van DNA-barcodes die kunnen worden gelezen met CRISPR-technologie.
Om deze aanpak te laten werken, moesten de onderzoekers een chemische modificatie gebruiken, fosforothioaat genaamd, om te voorkomen dat de circulerende DNA-reporter-streepjescodes in het bloed worden afgebroken. Deze modificatie is al gebruikt om de stabiliteit van moderne RNA-vaccins te verbeteren, waardoor ze langer in het lichaam kunnen overleven.
Net als bij de peptidereporters is elke DNA-streepjescode aan een nanodeeltje bevestigd door een linker die kan worden gesplitst door een specifiek protease. Als dat protease aanwezig is, komt het DNA-molecuul vrij en kan het vrij circuleren, om uiteindelijk in de urine terecht te komen. Voor deze studie gebruikten de onderzoekers twee verschillende soorten nanodeeltjes: één, een deeltje gemaakt van polymeren die door de FDA zijn goedgekeurd voor gebruik bij mensen, en de andere een “nanobody” – een antilichaamfragment dat kan worden ontworpen om zich op te hopen op een bepaald moment. tumor plaats.
Zodra de sensoren in de urine zijn uitgescheiden, kan het monster worden geanalyseerd met behulp van een papieren strook die een reporter herkent die wordt geactiveerd door een CRISPR-enzym genaamd Cas12a. Wanneer een bepaalde DNA-streepjescode in het monster aanwezig is, versterkt Cas12a het signaal zodat het kan worden gezien als een donkere strook op een papieren test.
De deeltjes kunnen worden ontworpen om veel verschillende DNA-streepjescodes te dragen, die elk een ander type proteaseactiviteit detecteren, wat “gemultiplexte” detectie mogelijk maakt. Het gebruik van een groter aantal sensoren zorgt voor een boost in zowel sensitiviteit als specificiteit, waardoor de test gemakkelijker onderscheid kan maken tussen tumortypes.
Ziekte handtekeningen
In tests met muizen toonden de onderzoekers aan dat een panel van vijf DNA-streepjescodes tumoren die voor het eerst in de longen ontstonden, nauwkeurig kon onderscheiden van tumoren gevormd door colorectale kankercellen die waren uitgezaaid naar de longen.
“Ons doel hier is om ziektesignaturen op te bouwen en om te zien of we deze streepjescodepanelen kunnen gebruiken om niet alleen een ziekte uit te lezen, maar ook om een ziekte te classificeren of om verschillende soorten kanker te onderscheiden”, zegt Hao.
Voor gebruik bij mensen verwachten de onderzoekers dat ze mogelijk meer dan vijf streepjescodes nodig hebben omdat er zoveel variatie is tussen de tumoren van patiënten. Om dat doel te helpen bereiken, werkten ze samen met onderzoekers van het Broad Institute of MIT en Harvard onder leiding van Harvard University Professor Pardis Sabeti, om een microfluïdische chip te maken die kan worden gebruikt om tot 46 verschillende DNA-barcodes uit één monster te lezen.
Dit soort testen kan niet alleen worden gebruikt om kanker op te sporen, maar ook om te meten hoe goed de tumor van een patiënt op de behandeling reageert en of de tumor na de behandeling is teruggekeerd. De onderzoekers werken nu aan het doorontwikkelen van de deeltjes met als doel ze op mensen te testen. Glympse Bio, een bedrijf dat mede is opgericht door Bhatia, heeft klinische fase 1-onderzoeken uitgevoerd met een eerdere versie van de urinaire diagnostische deeltjes en heeft vastgesteld dat deze veilig zijn bij patiënten.
Meer informatie:
Liangliang Hao et al, CRISPR-Cas-geamplificeerde urinaire biomarkers voor gemultiplexte en draagbare kankerdiagnostiek, Natuur Nanotechnologie(2023). DOI: 10.1038/s41565-023-01372-9
Tijdschrift informatie:
Natuur Nanotechnologie
Aangeboden door Massachusetts Institute of Technology