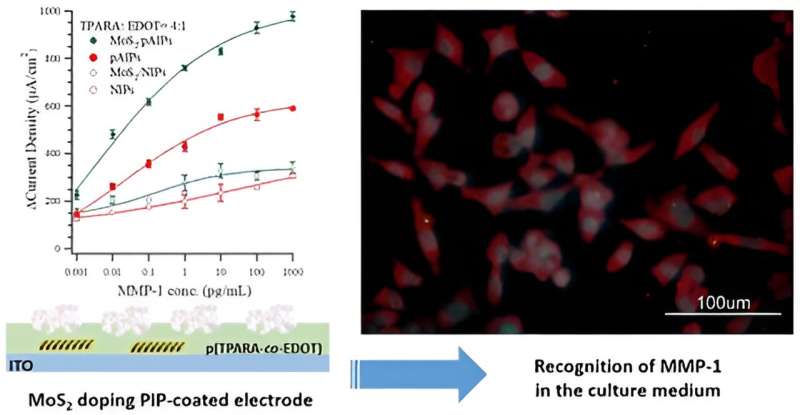
Grafisch abstract. Credit: ACS toegepaste nanomaterialen (2023). DOI: 10.1021/acsanm.3c04130
Patiënten die met sommige chronische ziekten worstelen, moeten vaak jaren wachten op een juiste diagnose. Symptomen zoals kortademigheid kunnen bijvoorbeeld worden toegeschreven aan veel long- en cardiovasculaire aandoeningen, zodat patiënten kunnen worden behandeld voor een verkeerd gediagnosticeerde ziekte die verre van nauwkeurige diagnose en behandeling is.
Daarom is een van de meest veelbelovende methoden om dit probleem aan te pakken het volgen van de niveaus van specifieke verbindingen in het lichaam tijdens de ontwikkeling van een specifieke ziekte. In deze richting presenteerden wetenschappers van het Instituut voor Fysische Chemie van de Poolse Academie van Wetenschappen (Warschau, Polen) en de Nationale Kaohsiung Universiteit in Kaohsiung (Kaohsiung, Taiwan) hun onderzoek naar de ontwikkeling van een methode voor snelle en effectieve diagnose van een dodelijke ziekte. longziekte.
Idiopathische longfibrose (IPF) is een chronische ziekte die longfibrose veroorzaakt met fatale gevolgen en tot verstikking. De meest voorkomende symptomen zijn droge hoest en kortademigheid, die met meerdere aandoeningen gepaard kunnen gaan. Er kan dus vaak een verkeerde diagnose worden gesteld bij veel verschillende ziekten, waardoor een nauwkeurige diagnose lang en lastig kan zijn, wat een dramatische invloed heeft op de levenskwaliteit van een patiënt.
Bovendien kunnen de symptomen worden uitgesteld totdat het te laat is om de patiënt succesvol te behandelen. De ontwikkeling van IPF is nog steeds een medisch mysterie. Daarom is er een enorme behoefte aan een vroege diagnose van IPF. Elektrochemische detectie van IPF-biomarkers is een van de oplossingen. Biomarkers zijn specifieke verbindingen, bijvoorbeeld eiwitten, nucleïnezuren of andere verbindingen die abnormaal door het lichaam worden geproduceerd tijdens de ontwikkeling van ziekten. Voor IPF kunnen verschillende biomarkers worden onderscheiden.
Eén daarvan is matrixmetalloproteïnase-1 (MMP-1), dat fibrillaire collagenen in de luchtwegen afbreekt. Ondanks de bekende chemische eigenschappen van MMP-1 is snelle monitoring van deze biomarker in lichaamsvloeistoffen als onderdeel van de IPF-progressie nu verre van een droomdiagnose.
Onlangs hebben onderzoekers van het Instituut voor Fysische Chemie van de Poolse Academie van Wetenschappen (IPC PAS) in Warschau (Polen), in samenwerking met wetenschappers van de afdeling Chemische en Materiaalkunde van de Nationale Kaohsiung Universiteit in Kaohsiung (Taiwan), zich gericht op snelle IPF en snelle diagnostiek volgen door een nieuwe elektrochemische chemosensor te ontwerpen voor selectieve, snelle en efficiënte bepaling van de IPF-biomarker, in het bijzonder MMP-1.
Om deze chemosensor te bereiden, vertrouwden de onderzoekers op moleculaire imprinting in polymeren, een techniek gebaseerd op het mengen van een functioneel monomeer, een verknopingsmiddel en een sjabloon, gevolgd door het genereren van een polymeermatrix die (sjabloonmolecuul)-vormige moleculaire holtes vormt die overeenkomen met een moleculaire sleutel die in het polymeerslot past.
Concreet hebben ze de transparante elektrode (een glasplaatje bedekt met het geleidende indium-tinoxide genaamd ITO) gemodificeerd met een moleculair bedrukt polymeer (MIP), poly (TPARA-co-EDOT), gemaakt van twee monomeren, EDOT en TPARA. Bovendien gedoteerd met een MoS2-2D-schilferig materiaal, de MIP werd getemperd met de peptide-epitoop van de MMP-1-eiwitbiomarker.
Vervolgens werd dit sjabloon uit de MIP verwijderd, waardoor moleculaire holten achterbleven met een vorm en grootte die kenmerkend zijn voor de peptide-epitoopmoleculen die voor het inprenting worden gebruikt. Omdat de holten overeenkomen met deze karakteristieke peptidemoleculen, kan de MIP eenvoudig worden gebruikt om het bijpassende molecuul te bepalen. Intrigerend genoeg is het doteren van de MIP met MoS2 verbeterde de MMP-1-detectielimiet aanzienlijk vergeleken met de ongedoteerde MIP.
Dr. Piyush S. Sharma beweert: “Het opnemen van nieuwe materialen in elektrochemische chemosensoren kan hun prestaties verbeteren en hun detectiemechanisme helpen ophelderen. In ons onderzoek werd MIP met (peptide-epitoop)-sjabloon gedoteerd met MoS2 vlokken met een gemiddelde grootte van 0,6 − 1,5 μm tijdens de afzetting ervan als een dunne film op een ITO-elektrode. In wezen verdubbelde deze doping de elektrochemische respons (boven de achtergrond) op de beoogde MMP-1-eiwitbiomarker.”
Het MMP-1-macromolecuul heeft verschillende peptiden aan de randen, de zogenaamde epitopen, die door het immuunsysteem worden herkend. Deze epitopen kunnen met succes worden gebruikt als afdruk in elektrochemische MIP-chemosensoren. Omdat het inprenting van eiwitten niet zou resulteren in hun succesvolle bepaling, wat zou leiden tot grote holtes waarin veel verbindingen met kleinere moleculen passen, waren de ingeprinte moleculen van een peptide-epitoop, veel kleiner dan eiwitten.
Bovendien zijn peptiden, naast hun kleinere omvang, stabieler dan eiwitten onder experimentele omstandigheden, inclusief het gebruik van een organisch oplosmiddel bij het vormen van een polymeerfilm op het elektrodeoppervlak. Het is vermeldenswaard dat het gebruik van MoS2 flakes maakt de detectie van de MMP-1-biomarker mogelijk en daarmee idiopathische longfibrose.
“De MoS2-gedoteerde pAIPs filmomhulde elektrodeprestaties zijn vergelijkbaar met de recente literatuur. Ten slotte werd de elektrode gebruikt om MMP-1 te bepalen in de kweekmedia van gen-bewerkte HEK293T-cellen en, vergeleken met een commerciële ELISA-test, was de nauwkeurigheid ervan hoog”, merkt prof. Włodzimierz Kutner op.
Dit onderzoek, gedetailleerd in ACS toegepaste nanomaterialen, is veelbelovend voor het monitoren van de ontwikkeling van chronische en progressieve ziekten met onbekende etiologie en pathogenese, waaronder idiopathische longfibrose.
Er is nog steeds ruimte voor het testen van detectie onder ontwrichtende omstandigheden, maar hopelijk zal moleculaire inprenting in polymeren meer aandacht en toepassing krijgen in de biogeneeskunde, waardoor de samenleving dichter bij een snelle en nauwkeurige diagnose van veel uitdagende ziekten komt. De onderzoekers hopen dat hun beproefde concept van een moleculair ingeprinte elektrochemische chemosensor ook kan worden aangepast aan andere ziekten en gepersonaliseerde geneeskunde.
Meer informatie:
Mei-Hwa Lee et al, MoS2 Nanosheet-gedoteerde peptide-bedrukte polymeer-gecoate elektroden voor elektrochemische bepaling van CRISPR/dCas9-geactiveerde eiwitexpressie, ACS toegepaste nanomaterialen (2023). DOI: 10.1021/acsanm.3c04130
Geleverd door de Poolse Academie van Wetenschappen