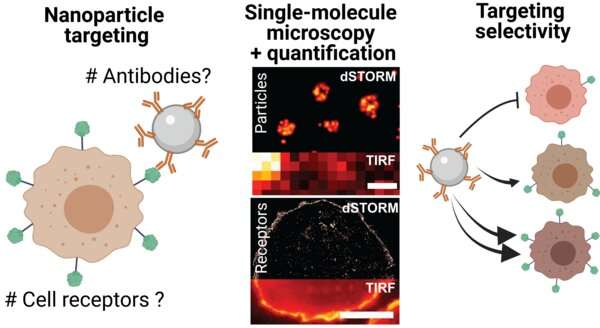
Credit: ontleend aan ‘A Single-Molecule View at Nanoparticle Targeting Selectivity: Correlation Ligand Functionality and Cell Receptor Density’. (https://pubs.acs.org/doi/10.1021/acsnano.1c08277.)
Nanodeeltjes kunnen worden gebruikt als krachtige voertuigen om vaccins toe te dienen en ernstige ziekten te voorkomen, zoals bij de behandeling van COVID-19, en om chemotherapeutische geneesmiddelen aan kankercellen te leveren met als doel de kankercellen uit te roeien en de gezonde cellen ongedeerd te laten. Voor kankerpatiënten heeft dit de potentie om ernstige bijwerkingen te verminderen die het gevolg zijn van de toxiciteit van chemotherapeutica. Helaas bestaat er nog geen klinisch toegepaste selectieve behandeling met nanodeeltjes (ook bekend als nanotherapeutisch), waarbij het onderzoek gericht is op het verbeteren en begrijpen van de huidige nanotherapeutica. Voor haar Ph.D. onderzoek nam Laura Woythe nanodeeltjes en kankercellen onder de loep om selectieve nanotherapeutica te ontwerpen met behulp van geavanceerde optische microscopietechnieken.
Om het vermogen van nanodeeltjes om kankercellen te targeten te vergroten, kunnen wetenschappers benutten hoe nanodeeltjes interageren met specifieke celbiomarkers of “receptoren” op het oppervlak van cellen. Hiervoor worden op het oppervlak van de nanodeeltjes moleculen of “liganden” geplaatst die specifieke celreceptoren herkennen.
Dit zogenaamde functionaliseringsproces is echter moeilijk te controleren, vanwege de kleine omvang van de nanodeeltjes, waardoor sommige moleculen misplaatst zijn, niet goed functioneren of zich per ongeluk op het oppervlak van de nanodeeltjes hechten. Al deze verminderen het vermogen van een nanodeeltje om op de beoogde manier met kankercellen te interageren.
Bovendien blijven er vragen over de efficiëntie van dergelijke hechtingsprotocollen en of het aantal moleculen dat we hechten efficiënt genoeg is om kankercellen te targeten. De uitdagingen liggen in de kleine omvang van de moleculen en celreceptoren, en de beperkte kwantitatieve methoden die beschikbaar zijn om het aantal moleculen op het oppervlak van de nanodeeltjes te schatten. Met andere woorden, hoe kunnen wetenschappers het aantal moleculen op het oppervlak van de nanodeeltjes tellen om te controleren of de nanodeeltjes effectief kunnen zijn tegen kankercellen?
Superresolutiemicroscopie
Voor haar Ph.D. onderzoek onderzocht Laura Woythe de functionaliteit van moleculen die aan nanodeeltjes zijn gehecht voor selectieve kankertargeting met behulp van geavanceerde optische microscopietechnieken of “superresolutie” optische microscopie.
Superresolutiemicroscopie omvat een groep microscopietechnieken met een resolutievermogen dat 10 keer hoger is dan conventionele optische microscopie. Dit maakt de visualisatie van nanometrische structuren, zoals nanodeeltjes en celreceptoren, in het bereik van 10 tot 100 nanometer (nm) mogelijk. Dit groottebereik staat gelijk aan het visualiseren van structuren die tot 5.000 keer kleiner zijn dan een mensenhaar.
Met behulp van superresolutiemicroscopie waren Woythe en haar collega’s in staat om individuele liganden op nanodeeltjes en receptoren op kankercellen te tellen, waardoor de targeting-interactie kon worden verfijnd. Deze cijfers kunnen een grote bijdrage leveren aan de ontwikkeling van efficiëntere nanotherapeutische toediening.
Het onderzoek van Woythe is een belangrijke stap op weg naar een beter begrip van nanomaterialen voor biomedische toepassingen, met name selectieve celtargeting van kankercellen en zieke cellen zonder gezond weefsel aan te tasten, en zo de mogelijke bijwerkingen en de belasting die dit voor kankerpatiënten veroorzaakt te minimaliseren.
Moleculaire mapping van targeting van nanodeeltjes: een super-opgeloste reis. research.tue.nl/en/publication … -super-resolved-jour
Laura Woythe et al, A Single-Molecule View at Nanoparticle Targeting Selectivity: Correlation Ligand Functionality and Cell Receptor Density, ACS Nano (2022). DOI: 10.1021/acsnano.1c08277
ACS Nano
Aangeboden door de Technische Universiteit Eindhoven