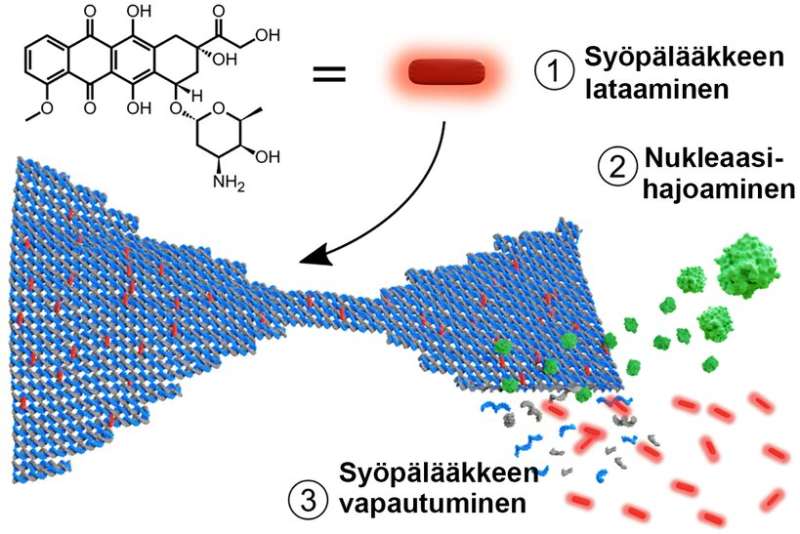
Anti-kanker Dox-moleculen (rood) worden via intercalatie in DNA-origami-nanostructuren (blauwe vlinderdas) geladen. 2) DNA-origami wordt verteerd door endonuclease (groen). 3) Terwijl de origami wordt opgesplitst in korte enkelstrengige fragmenten, komt de Dox vrij in de omgeving. Krediet: Aalto University
DNA-nanotechnologie – het onderzoeksveld dat DNA-moleculen als bouwmateriaal gebruikt – heeft zich de afgelopen jaren snel ontwikkeld en heeft de constructie van steeds complexere nanostructuren mogelijk gemaakt. DNA-nanostructuren, zoals DNA-origami, dienen als een uitstekende basis voor op nanodragers gebaseerde toepassingen voor medicijnafgifte, en voorbeelden van hun gebruik bij medische behandelingen zijn al aangetoond. Hoewel de stabiliteit van dergelijke DNA-nanostructuren onder fysiologische omstandigheden kan worden verbeterd, is er weinig bekend over hun vertering door endonucleasen, die, overal in ons bloed en weefsels aangetroffen, verantwoordelijk zijn voor het vernietigen van vreemd DNA in ons lichaam.
Om deze opkomende vraag aan te pakken, heeft een team van onderzoekers van de Aalto University (Finland), de University of Jyväskylä (Finland), Ludwig-Maximilian-Universität München (Duitsland) en Universität Paderborn (Duitsland) een manier gevonden om de endonuclease-aangedreven vertering van met medicijnen beladen DNA-nanostructuren in realtime.
De eerdere experimenten van de onderzoekers gebruikten atoomkrachtmicroscopie met hoge snelheid om aan te tonen dat het ontwerp van DNA-origami een rol speelt in hoe snel ze uit elkaar vallen in een endonucleaserijke omgeving. Hoewel ze het verteringsproces op het niveau van een enkele structuur konden volgen, was de benadering beperkt tot tweedimensionale DNA-origami-vormen die op een microscoopsubstraat waren afgezet.
Nu heeft de groep de DNA-afbraak gevolgd en de daaropvolgende afgifte van het antikankermedicijn doxorubicine (Dox) uit de DNA-structuren. Het medicijn bindt tussen DNA-basenparen.
“We observeerden zowel de verteringsprofielen als het medicijnafgifteprofiel, aangezien het medicijn vrijkomt na DNA-fragmentatie door nucleasen, en belangrijker nog, in de oplossingsfase. Met deze methode kunnen we het collectieve gedrag van alle nanostructuren zien wanneer ze vrij in vloeistof zweven. ‘, zegt Adjunct Professor Veikko Linko van de Aalto University, die de studie leidde.
“Het lijkt erop dat de vertering anders gebeurt op substraten en in oplossing, en door deze twee soorten informatie te combineren, kunnen we beter begrijpen hoe de nanostructuren worden verteerd door nucleasen in de bloedbaan. Bovendien toonden we aan dat de profielen van geneesmiddelafgifte nauw verband hielden met de verteringsprofielen en een breed scala aan geneesmiddeldoses kunnen worden bereikt door simpelweg de vorm of geometrie van de DNA-nanostructuur te veranderen ”, legt promovendus Heini Ijäs, de hoofdauteur van het onderzoek, uit.
Toen het team de binding van Dox aan de DNA-structuren tot in detail onderzocht, ontdekten ze dat de meeste eerdere onderzoeken de laadcapaciteit van Dox van DNA-origami enorm hebben overschat.
“De antikankereffecten van met Dox uitgeruste DNA-nanostructuren zijn in veel publicaties gerapporteerd, maar het lijkt erop dat deze effecten voornamelijk zijn veroorzaakt door vrije of geaggregeerde Dox-moleculen, niet door de met medicijnen beladen DNA-motieven. We geloven dat dit soort informatie is cruciaal voor de ontwikkeling van veilige en effectievere medicijnafgiftesystemen, en brengt ons een stap dichter bij real-world op DNA gebaseerde biomedische toepassingen ”, zegt Ijäs.
Ontrafelen van de interactie tussen doxorubicine en DNA-origami-nanostructuren voor aanpasbare chemotherapeutische medicijnafgifte. Onderzoek naar nucleïnezuren doi.org/10.1093/nar/gkab097
Onderzoek naar nucleïnezuren
Geleverd door Aalto University