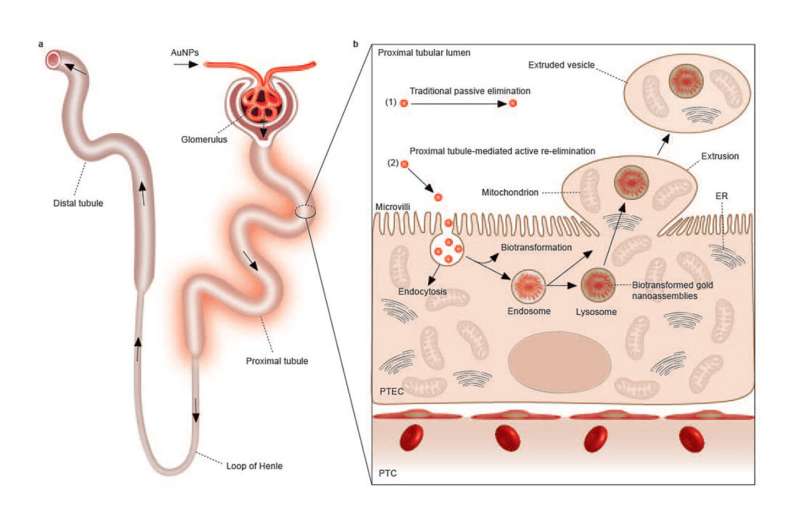
Onderzoekers ontdekten een ‘huishouding’-methode die niercellen gebruiken om cellulaire inhoud te verwijderen en zichzelf te vernieuwen, zonder dat celdeling nodig is. Ze bestudeerden hoe gouden nanodeeltjes (AuPT’s) door de proximale tubuli van de nier reizen, waar cellen de deeltjes opnemen en in lysosomen omsluiten. De proximale buisvormige cellen vormen naar buiten gerichte uitstulpingen in hun membranen die de AuPT’s, lysosomen, mitochondria, endoplasmatisch reticulum en andere organellen bevatten die doorgaans beperkt zijn tot het inwendige van een cel. De geëxtrudeerde inhoud wordt vervolgens afgeknepen in een blaasje dat wegdrijft in de extracellulaire ruimte. Credit: Natuur Nanotechnologie (2023). DOI: 10.1038/s41565-023-01366-7
Wetenschappers van de Universiteit van Texas in Dallas hebben een tot nu toe onbekend ‘huishoudingsproces’ in niercellen ontdekt dat ongewenste inhoud uitwerpt, wat resulteert in cellen die zichzelf verjongen en blijven functioneren en gezond blijven.
Het zelfvernieuwingsproces, dat fundamenteel verschilt van de manier waarop ander lichaamsweefsel wordt verondersteld te regenereren, helpt verklaren hoe de nieren, behoudens letsel of ziekte, een leven lang gezond kunnen blijven. De onderzoekers beschreven het mechanisme in een studie die op 17 april werd gepubliceerd Natuur Nanotechnologie.
In tegenstelling tot de lever en de huid, waar cellen zich delen om nieuwe dochtercellen te creëren en het orgaan te regenereren, zijn cellen in de proximale tubuli van de nier mitotisch in rust – ze delen niet om nieuwe cellen te creëren. In gevallen van lichte verwonding of ziekte hebben niercellen beperkte herstelmogelijkheden en kunnen stamcellen in de nier nieuwe niercellen vormen, maar slechts tot op zekere hoogte, zei Dr. Jie Zheng, professor scheikunde en biochemie aan de School of Natuurwetenschappen en Wiskunde en co-corresponderende auteur van de studie.
“In de meeste scenario’s, als niercellen ernstig gewond raken, zullen ze sterven en kunnen ze niet regenereren”, zegt Zheng, een Distinguished Chair in Natural Sciences and Mathematics. “Je nier zal vroeg of laat gewoon falen. Dat is een grote uitdaging in het gezondheidsmanagement van nierziekte. Alles wat we momenteel kunnen doen, is de progressie naar nierfalen vertragen. We kunnen het orgaan niet gemakkelijk repareren als het ernstig gewond is of door een chronische ziekte.
“Daarom is de ontdekking van dit zelfvernieuwingsmechanisme waarschijnlijk een van de belangrijkste bevindingen die we tot nu toe hebben gedaan. Met uitstekende kernfaciliteiten en toegewijd personeel is UTD een geweldige plek om dergelijk baanbrekend onderzoek te doen.”
Verder onderzoek kan leiden tot verbeteringen in nanogeneeskunde en vroege opsporing van nieraandoeningen, zei hij.
Een onverwachte bevinding
De onderzoekers zeiden dat hun ontdekking hen verraste.
Al 15 jaar onderzoekt Zheng het biomedische gebruik van gouden nanodeeltjes als beeldvormende middelen, voor fundamenteel begrip van glomerulaire filtratie, voor vroege detectie van leverziekte, en voor gerichte levering van geneesmiddelen tegen kanker. Een deel van dat werk was gericht op het begrijpen van hoe gouden nanodeeltjes door de nieren worden gefilterd en via de urine uit het lichaam worden verwijderd.
Onderzoek heeft aangetoond dat gouden nanodeeltjes over het algemeen ongeschonden door een structuur in de nier, de glomerulus genaamd, gaan en vervolgens in de proximale tubuli terechtkomen, die meer dan 50% van de nier uitmaken. Van proximale tubulaire epitheelcellen is aangetoond dat ze de nanodeeltjes internaliseren, die uiteindelijk aan die cellen ontsnappen om in de urine te worden uitgescheiden. Maar hoe ze uit de cellen ontsnappen, is onduidelijk.
In december 2021 hebben Zheng en zijn scheikundeteam – onderzoeker en hoofdonderzoeksauteur Yingyu Huang Ph.D. ’20 en co-corresponderende auteur Dr. Mengxiao Yu, universitair hoofddocent, onderzochten gouden nanodeeltjes in proximale tubulaire weefselmonsters met behulp van een optische microscoop, maar schakelden over op een van de elektronenmicroscopen (EM) van de universiteit voor een betere resolutie.
“Met behulp van de EM zagen we gouden nanodeeltjes ingekapseld in lysosomen in grote blaasjes in het lumen, de ruimte buiten de epitheelcellen, ” zei Yu.
Blaasjes zijn kleine met vloeistof gevulde zakjes die zowel binnen als buiten cellen worden aangetroffen en die verschillende stoffen transporteren.
“Maar we hebben ook de vorming waargenomen van deze blaasjes die zowel nanodeeltjes als organellen buiten cellen bevatten, en het was niet iets dat we eerder hadden gezien, ” zei Yu.
De onderzoekers vonden proximale tubulaire cellen die naar buiten gerichte uitstulpingen hadden gevormd in hun luminale membranen die niet alleen gouden nanodeeltjes bevatten, maar ook lysosomen, mitochondria, endoplasmatisch reticulum en andere organellen die typisch beperkt zijn tot het inwendige van een cel. De geëxtrudeerde inhoud werd vervolgens afgeknepen in een blaasje dat wegdreef in de extracellulaire ruimte.
“Op dat moment wisten we dat dit een ongewoon fenomeen was”, zei Yu. “Dit is een nieuwe methode voor cellen om cellulaire inhoud te verwijderen.”
Een nieuw vernieuwingsproces
Het extrusie-gemedieerde zelfvernieuwingsmechanisme verschilt fundamenteel van andere bekende regeneratieve processen, zoals celdeling, en schoonmaaktaken zoals exocytose. Bij exocytose worden vreemde stoffen zoals nanodeeltjes ingekapseld in een blaasje in de cel. Vervolgens versmelt het blaasjemembraan met de binnenkant van het celmembraan, dat opent om de inhoud naar buiten af te geven.
“Wat we ontdekten, is totaal anders dan het eerdere begrip van hoe cellen deeltjes elimineren. Er is geen membraanfusie in het extrusieproces, waardoor oude inhoud van normale cellen wordt verwijderd en de cellen zichzelf kunnen updaten met nieuwe inhoud, ” zei Huang. “Het gebeurt of er nu vreemde nanodeeltjes aanwezig zijn of niet. Het is een intrinsiek, proactief proces dat deze cellen gebruiken om langer te overleven en goed te functioneren.”
Zheng zei dat hun bevindingen nieuwe studiegebieden openen. Epitheelcellen, zoals die in de proximale tubuli, worden bijvoorbeeld aangetroffen in andere weefsels, zoals de wanden van slagaders en in de darm en het spijsverteringskanaal.
“Op het gebied van nanogeneeskunde willen we de ophoping van nanodeeltjes in het lichaam zoveel mogelijk minimaliseren. We willen niet dat ze vast komen te zitten in de nieren, dus het is erg belangrijk om te begrijpen hoe nanodeeltjes worden geëlimineerd uit de proximale tubuli, ‘ zei Zheng. “Ook als we zouden kunnen leren hoe we dit zelfvernieuwingsproces kunnen reguleren of controleren, kunnen we een manier vinden om de nieren gezond te houden bij patiënten met hoge bloeddruk of diabetes.
“Als we manieren zouden kunnen ontwikkelen om de handtekening van dit proces niet-invasief te detecteren, zou het misschien een indicator kunnen zijn van vroege nierziekte.”
Meer informatie:
Yingyu Huang et al, Proximale tubuli elimineren geëndocyteerde gouden nanodeeltjes door een organel-extrusie-gemedieerd zelfvernieuwingsmechanisme, Natuur Nanotechnologie (2023). DOI: 10.1038/s41565-023-01366-7
Tijdschrift informatie:
Natuur Nanotechnologie
Aangeboden door de Universiteit van Texas in Dallas