
Fig. Schematische illustratie van met alkyn gelabelde detectie van kleine moleculen in levende cellen met behulp van oppervlakte-versterkte Raman-verstrooiing van gouden nanodeeltjes. Krediet: Osaka University
Succesvolle geneesmiddelenontwikkeling heeft een aanzienlijke impact op de kwaliteit van leven van mensen wereldwijd. In staat zijn om te volgen hoe moleculen in doelcellen terechtkomen en te observeren wat ze doen als ze binnen zijn, is de sleutel tot het identificeren van de beste kandidaten. Analysetechnieken vormen daarom een belangrijk onderdeel van het drug discovery-proces. Onderzoekers van de Universiteit van Osaka, in samenwerking met RIKEN, hebben een op Raman-microscopie gebaseerde benadering gerapporteerd voor het visualiseren van geneesmiddelen met kleine moleculen die gouden nanodeeltjes gebruiken. De bevindingen van het team zijn gepubliceerd in ACS Nano.
Kleine medicijnmoleculen worden vaak opgespoord door ze te bevestigen aan fluorescerende sondes die zichtbaar zijn wanneer ze met licht worden bestraald. Microscopie kan vervolgens worden gebruikt om deze moleculen in cellen in realtime te zien. Fluorescerende moleculen kunnen echter omvangrijk zijn, wat het gedrag van de kleine moleculen kan beïnvloeden. Bovendien verliezen sommige fluorescerende moleculen hun fluorescentie als ze worden blootgesteld aan te veel licht, waardoor het moeilijk wordt om ze te zien tijdens lange studies.
Een alternatief voor fluorescerende labels is een veel kleiner label dat bekend staat als een alkyn, dat is samengesteld uit drievoudige koolstof-koolstofbindingen. De bijzondere rangschikking van atomen in alkynen komt van nature niet voor in cellen; daarom bieden ze een zeer specifieke marker. Bovendien betekent hun kleine formaat dat alkynen een minimaal effect hebben op het gedrag van kleine moleculen. In plaats van fluorescentie onder laserlicht uit te zenden, produceren alkynen een zogenaamd Raman-signaal, dat duidelijk kan worden geïdentificeerd tussen de signalen van het celmateriaal.
Het zoeken naar het Raman-signaal van alkyngroepen is echter lastig als er niet veel in de buurt zijn vanwege de lage efficiëntie van Raman-verstrooiing. De onderzoekers hebben daarom alkyne-tagging gecombineerd met het gebruik van gouden nanodeeltjes. Surface-Enhanced Raman Scattering (SERS) microscopie kan gouden nanodeeltjes stimuleren om verbeterde elektrische velden te produceren die het Raman-signaal van de alkyngroepen versterken, waardoor ze gemakkelijker te detecteren zijn.
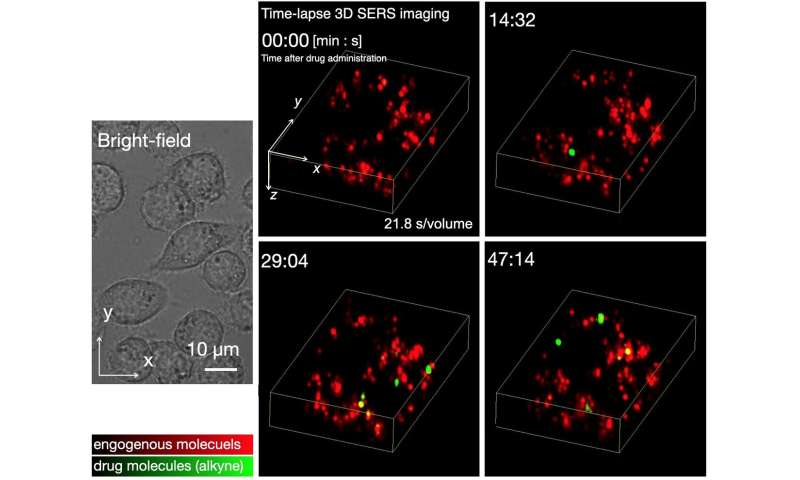
Fig. 2 Time-lapse 3D SERS-beeldvorming van opname van kleine moleculen door levende cellen. We hebben met succes waargenomen dat de SERS-signalen van alkynen aanvankelijk werden gedetecteerd rond 10-15 minuten na toediening van het geneesmiddel, en het aantal signalen nam geleidelijk toe met de tijd. De concentratie van geneesmiddelentoediening was 20 µM. Krediet: Osaka University
“Onze aanpak is een combinatie van technieken die zijn gebruikt voor het volgen van kleine moleculen in levende cellen”, legt hoofdauteur Kota Koike uit. “Gouden nanodeeltjes zijn bijzonder nuttige boodschappers om de aanwezigheid van alkyngroepen te melden, omdat ze het alkynsignaal versterken en een oppervlak bieden waar de alkynen graag interactie mee hebben. De twee componenten komen daarom op natuurlijke wijze samen om het verbeterde signaal te genereren.”
Gouden nanodeeltjes worden gemakkelijk opgenomen door tal van verschillende soorten cellen, waardoor de techniek breed toepasbaar is. De nanodeeltjes komen de lysosoomcompartimenten in de cel binnen en versterken vervolgens het signaal van de alkyn-gelabelde moleculen die vervolgens in de lysosomen aankomen en daarmee een interactie aangaan.
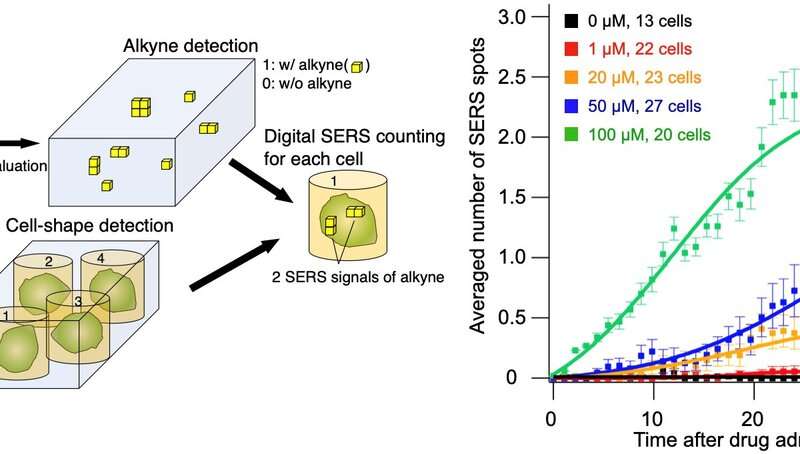
Fig. 3 Kwantitatieve detectie van het aantal SERS-signalen van alkynen op het eencellige niveau (linker figuur). Het aantal SERS-signalen dat per cel wordt gedetecteerd bij elke toedieningsconcentratie in de tijd (rechts). Met behulp van de kwantitatieve SERS-detectiemethode hebben we met succes vastgesteld dat de opnamesnelheid sterk afhing van de medicijnconcentratie. Krediet: Osaka University
“Onze SERS-techniek heeft het potentieel om te worden gebruikt met een verscheidenheid aan verschillende celtypen, evenals een vrijwel onbeperkt aantal kandidaat-geneesmiddelen”, legt de corresponderende auteur Katsumasa Fujita uit. “Dit is vooral spannend voor het ontdekken van geneesmiddelen, waar elk middel om de dynamiek van geneesmiddelen in realtime beter te begrijpen, buitengewoon waardevol is voor de ontwikkeling.”
Kota Koike et al. Kwantitatieve geneesmiddeldynamiek gevisualiseerd door plasmonisch-verbeterde Raman-microscopie met alkyn-tag, ACS Nano (2020). DOI: 10.1021 / acsnano.0c05010
ACS Nano
Geleverd door Osaka University