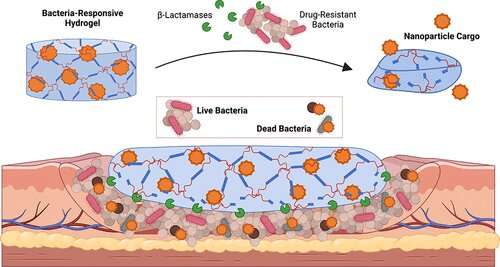
Krediet: Dahlia Alkekhia et al, ACS toegepaste materialen en interfaces (2022). DOI: 10.1021/acsami.2c02614
Een team van onderzoekers van de Brown University heeft een nieuw responsief materiaal ontwikkeld dat ingekapselde lading alleen kan vrijgeven als er pathogene bacteriën aanwezig zijn. Het materiaal zou kunnen worden gebruikt om wondverbanden te maken die snel reageren op ontluikende infecties, maar alleen medicatie op aanvraag afleveren.
De ontwikkeling is vooral relevant in het licht van de wereldwijde antibioticaresistentiecrisis, zeggen de onderzoekers, omdat het materiaal zou kunnen helpen infecties te bestrijden en tegelijkertijd het probleem van resistentie aan te pakken.
“We hebben een door bacteriën geactiveerd, slim medicijnafgiftesysteem ontwikkeld”, zegt Anita Shukla, universitair hoofddocent aan Brown’s School of Engineering, die de ontwikkeling van het materiaal leidde. “Onze hypothese is dat technologieën zoals deze, die de hoeveelheid medicijn verminderen die nodig is voor een effectieve behandeling, ook zowel bijwerkingen als het potentieel voor resistentie kunnen verminderen.”
Het nieuwe materiaal, beschreven in het tijdschrift ACS toegepaste materialen en interfaces, is een hydrogel – een gehydrateerd polymeernetwerk. Hydrogels zijn zeer biocompatibel en kunnen worden gebruikt om een reeks nanodeeltjes of therapieën met kleine moleculen in te kapselen. Ze worden vaak gebruikt in wondverbanden. “Slimme” of responsieve hydrogels zijn in opkomst als veelbelovende platforms voor medicijnafgifte. Ze kunnen worden gemaakt om te reageren op de plaatselijke omgeving – de afgifte van medicatie versnellen of vertragen als reactie op temperatuur, pH of andere factoren.
Voor dit nieuwe materiaal hebben Shukla en haar team een hydrogel ontwikkeld die gevoelig is voor β-lactamasen, een klasse enzymen die vrijkomen door een verscheidenheid aan schadelijke bacteriën. De aanwezigheid van β-lactamasen zorgt ervoor dat het verknoopte polymeernetwerk van het materiaal degradeert, waardoor de therapeutische nanodeeltjes vrijkomen die erin worden vastgehouden.
“Wat interessant is, is dat β-lactamasen eigenlijk een belangrijke oorzaak zijn van antibioticaresistentie, omdat ze β-lactam-antibiotica vernietigen, die enkele van onze meest voorgeschreven antibiotica zijn,” zei Shukla. “Maar we hebben dit bacteriële afweermechanisme gebruikt en het tegen de bacteriën gebruikt.”
In een reeks laboratoriumexperimenten toonden Shukla en een team van Brown-afgestudeerde studenten aan dat het materiaal inderdaad gevoelig is voor β-lactamasen, waarbij de lading van nanodeeltjes alleen vrijkomt als β-lactamasen of β-lactamase-producerende bacteriën aanwezig waren. Anders hield het materiaal zijn lading ingekapseld. Het team is van plan door te gaan met het ontwikkelen en testen van het materiaal, uiteindelijk in de klinische setting als een wondverband dat kan reageren op opkomende infecties.
“We denken dat dit iets is dat het potentieel heeft om naar de kliniek te worden vertaald,” zei Shukla. “Daar blijven we aan werken.”
Andere auteurs van het onderzoek zijn Dahlia Alkekhia en Cassi LaRose van Brown’s Center for Biomedical Engineering.
Dahlia Alkekhia et al, β-Lactamase-Responsive Hydrogel Drug Delivery Platform voor door bacteriën geactiveerde ladingvrijgave, ACS toegepaste materialen en interfaces (2022). DOI: 10.1021/acsami.2c02614
ACS toegepaste materialen en interfaces
Geleverd door Brown University