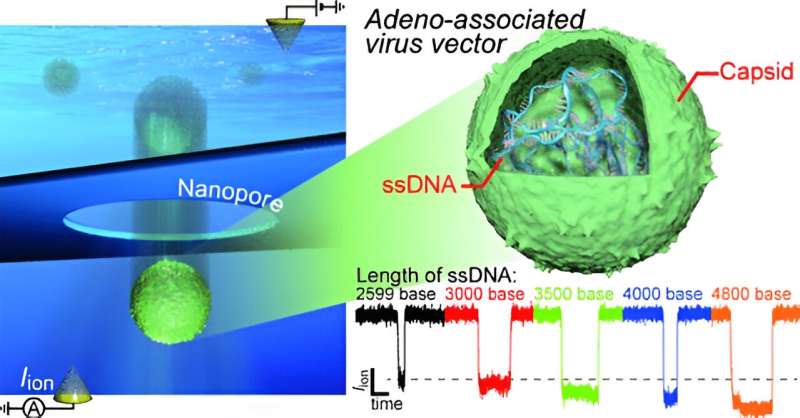
Credit: ACS Nano (2024). DOI: 10.1021/acsnano.4c01888
Virale vectoren hebben veel potentieel voor genbewerking en gentherapie, maar er is een dringende behoefte aan het ontwikkelen van kwaliteitscontrolemethoden om mogelijke bijwerkingen voor patiënten te minimaliseren. Om dit aan te pakken, ontwikkelden onderzoekers uit Japan een op nanosensoren gebaseerde aanpak die onderscheid kan maken tussen functionele en defecte virale vectoren op het niveau van één deeltje. Deze handige en goedkope techniek brengt ons hopelijk een stap dichter bij het verbeteren van behandelingen voor genetische aandoeningen.
De afgelopen decennia is er opmerkelijke vooruitgang geboekt in genetische manipulatietechnologieën, waardoor we dichter bij het punt komen waarop genen in vivo kunnen worden gemodificeerd. Dergelijke hulpmiddelen zouden de weg vrijmaken voor gentherapie en een nieuw tijdperk in de geneeskunde inluiden. Tot nu toe omvatten de meest veelbelovende strategieën voor gentherapie het benutten van de bestaande moleculaire machinerie die in virussen wordt aangetroffen.
Met name adeno-associated virus (AAV) vectoren hebben recentelijk veel aandacht gekregen van de wetenschappelijke gemeenschap, gezien hun potentieel om te dienen als nucleïnezuurvaccins voor ziekten zoals COVID-19. Echter, tijdens de productie van AAV vectoren kunnen sommige deeltjes slechts een gedeeltelijke kopie van het beoogde genoom bevatten, terwijl andere leeg kunnen zijn. Deze defecte vectoren kunnen leiden tot onverwachte bijwerkingen, wat de dringende behoefte aan robuuste kwaliteitscontrolemethoden in hun productie onderstreept.
Om deze uitdaging aan te pakken, rapporteerde een team van onderzoekers uit Japan onlangs een nieuwe nanosensortechniek om virale vectorkenmerken te meten. Hun bevindingen werden gepresenteerd in hun nieuwste paper, gepubliceerd online op 5 juni 2024, in ACS Nano.
Het team bestaat uit universitair hoofddocent Makusu Tsutsui en professor Tomoji Kawai van het Institute of Scientific and Industrial Research van de Universiteit van Osaka; docent Akihide Arima van het Institute of Nano-Life-Systems van de Universiteit van Nagoya; speciaal aangestelde professor Yoshinobu Baba van het Institute of Nano-Life-Systems Institutes of Innovation for Future Society van de Universiteit van Nagoya; projectonderzoeker Mikako Wada, universitair hoofddocent Yuji Tsunekawa en professor Takashi Okada, allen van het Institute of Medical Science van de Universiteit van Tokio.
De voorgestelde aanpak omvat het meten van de ionenstroom die door een nanopore-opening stroomt wanneer een spanningsverschil wordt toegepast op een oplossing die AAV’s bevat. Wanneer de nanopore niet wordt geblokkeerd, is de gemeten ionenstroom relatief constant. Maar wanneer een viraal deeltje door de nanopore passeert, wordt de ionenstroom gedeeltelijk geblokkeerd voor een kort moment, wat een piek of puls produceert in de ionenstroomuitlezing.
Interessant is dat AAV-vectoren met een volledig genoom zwaarder en iets omvangrijker zijn dan lege of gedeeltelijk gevulde vectoren. Hierdoor is het mogelijk om onderscheid te maken tussen de vectoren terwijl ze door de nanoporie gaan. Defecte vectoren produceren een ‘handtekening’ in de gemeten ionenstroom die merkbaar verschilt van die van vectoren met een volledig genoom.
Het team verifieerde dit door middel van experimenten, eindige-elementensimulaties en theoretische analyses. “Door een sensor te ontwerpen met een optimale structuur, identificeerden we voor het eerst de gen-afgeleide sub-nanometer-schaalverschillen in de grootte van de virale vectoren,” legt Tsutsui uit.
Deze techniek maakt een gemakkelijke en goedkope kwaliteitscontrole van AAV-vectoren mogelijk. Tot nu toe was dit afhankelijk van complexe methoden zoals massafotometrie, transmissie-elektronenmicroscopie en analytische ultracentrifugatie.
“Het huidige werk kan de geneeskunde revolutioneren door een hulpmiddel te bieden voor het voorbereiden van AAV-vectoren met ultrahoge kwaliteit voor veilige en effectieve gentherapie,” benadrukt Tsunekawa. “Het kan cruciaal zijn voor de ontwikkeling van productie- en zuiveringssystemen voor AAV-vectoren,” voegt hij toe.
Bovendien biedt deze aanpak, naast AAV-vectoren, perspectief voor het bestuderen van andere typen virale vectoren, wat mogelijk nieuwe wegen opent voor effectieve gentherapieën en ons begrip van virale biologie vergroot. Bovendien zou het garanderen van de hoge kwaliteit van klinisch gebruikte AAV-vectoren kunnen zorgen voor lagere patiëntdoses, waardoor bijwerkingen worden geminimaliseerd.
Meer informatie:
Makusu Tsutsui et al, Identificatie van virale vectorkenmerken door nanopore-detectie, ACS Nano (2024). DOI: 10.1021/acsnano.4c01888
Tijdschriftinformatie:
ACS Nano
Aangeboden door de Universiteit van Tokio