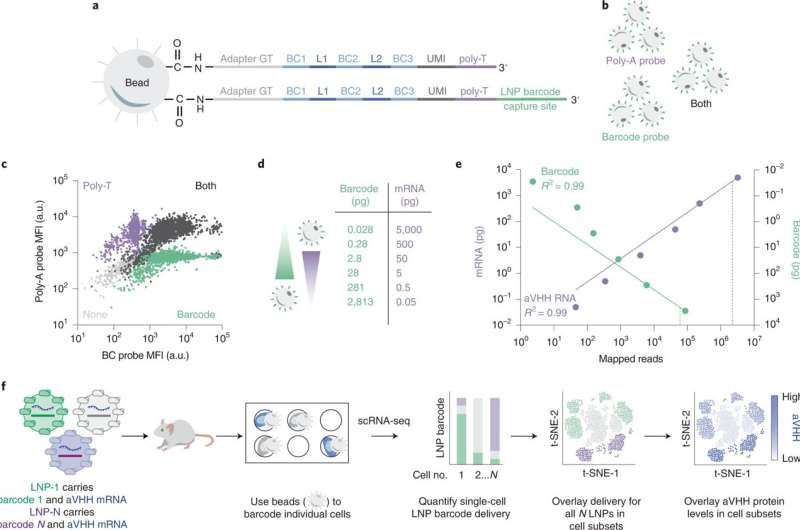
SENT-seq gebruikt orthogonale opnamesequenties om afstembare multiomische uitlezingen te genereren. Credit: Natuur Nanotechnologie (2022). DOI: 10.1038/s41565-022-01146-9
Therapeutica op basis van boodschapper-RNA, of mRNA, kunnen potentieel een breed scala aan ziekten behandelen, waaronder kanker, genetische ziekten en, zoals de wereld de afgelopen jaren heeft geleerd, dodelijke virussen.
Om te werken, moeten deze medicijnen rechtstreeks aan de doelcellen worden afgeleverd in bubbels van vet op nanoschaal die lipidenanodeeltjes of LNP’s worden genoemd – mRNA is niet veel goeds als het niet het juiste celtype bereikt.
Een team van onderzoekers van het Georgia Institute of Technology en de Emory University’s School of Medicine heeft een nieuwe stap gezet in de richting van het verbeteren van de ontwikkeling van deze op maat gemaakte leveringsvoertuigen, en rapporteert hun werk op 30 juni in Natuur Nanotechnologie. Curtis Dobrowolski en Kalina Paunovska, stagiaires in het lab van James Dahlman, hebben een systeem ontwikkeld om preklinische nanodeeltjesstudies voorspellender te maken. Hun ontdekkingen beïnvloeden nu al de richting van het onderzoek in dit groeiende, competitieve veld.
“Ik ben erg enthousiast over deze studie en verwacht dat we de meeste van onze toekomstige projecten naar deze methodologie zullen verschuiven”, zegt Dahlman, universitair hoofddocent en McCamish Foundation Early Career Professor in de Wallace H. Coulter Department of Biomedical Engineering aan Georgia Tech en Emory.
Opeenvolging van gebeurtenissen
De afgelopen jaren werkte Dahlman samen met Coulter BME-professor Philip Santangelo in een druk onderzoeksbedrijf. Het laboratorium van Santangelo ontwikkelt mRNA-therapieën en het laboratorium van Dahlman levert het met behulp van LNP’s.
Om het proces van het testen van de effectiviteit van hun LNP’s te versnellen, heeft het team van Dahlman een techniek ontwikkeld die DNA-barcoding wordt genoemd. In dit proces voegen onderzoekers een stukje DNA in dat overeenkomt met een bepaalde LNP. De LNP’s worden vervolgens geïnjecteerd en cellen worden vervolgens onderzocht op de aanwezigheid van de “barcodes” met behulp van genetische sequencing. Het systeem identificeert welke streepjescodes welke specifieke doelen hebben bereikt en benadrukt de meest veelbelovende nanodeeltjes. Omdat veel DNA-sequenties tegelijk kunnen worden gelezen, maakt het barcoderingsproces het mogelijk om veel experimenten tegelijkertijd uit te voeren, waardoor de ontdekking van effectieve dragers van lipidenanodeeltjes wordt versneld.
DNA-barcodering heeft het preklinische screeningproces van nanodeeltjes aanzienlijk verbeterd. Maar er is nog steeds een belangrijke barrière die de toediening van medicijnen beïnvloedt. Vanwege hun diversiteit zijn cellen een soort bewegende doelen. Dahlman merkte op dat cellen die eerder als homogeen werden beschouwd, zijn samengesteld uit verschillende en gevarieerde celsubsets. Zijn team vermoedde dat deze chemische en genetische heterogeniteit een krachtige invloed heeft op hoe goed LNP’s mRNA-therapieën in de cellen kunnen afleveren.
“Cellen hebben niet slechts één eiwit dat ze definieert – ze zijn gecompliceerd,” zei Dahlman. “Ze kunnen worden gedefinieerd door een combinatie van dingen, en als we eerlijk zijn, kunnen ze het beste worden gedefinieerd met behulp van alle genen die ze wel of niet tot expressie brengen.”
Om hun hypothese te testen, ontwikkelden de onderzoekers een nieuwe tool om al deze dingen tegelijk te meten. Hun multiomic nanodeeltjesafgiftesysteem wordt single-cell nanoparticle targeting-sequencing of SENT-seq genoemd.
Multiomics-benadering
Met behulp van SENT-seq konden de onderzoekers kwantificeren hoe LNP’s DNA-barcodes en mRNA in cellen afleveren, de daaropvolgende eiwitproductie mogelijk gemaakt door het mRNA-medicijn, evenals de identiteit van de cel, in duizenden individuele cellen.
Deze multiomics-aanpak zou een belangrijke sprong voorwaarts kunnen betekenen voor LNP-ontdekking met hoge doorvoer. Dankzij de SENT-seq-techniek kon het team celsubtypes identificeren die een bijzonder hoge of lage opname van nanodeeltjes vertonen, en de genen die bij die subtypes horen.
Dus, naast het testen van de werkzaamheid van een medicijn en hoe bepaalde celsubtypes reageren op nanodeeltjes, identificeren ze welke genen betrokken zijn bij de succesvolle opname van LNP’s. En ze doen het allemaal tegelijk.
“De gegevens suggereren dat deze verschillende celsubsets verschillende reacties hebben op nanodeeltjes die van invloed zijn op hoe goed een mRNA-therapie werkt,” zei Dahlman. “Er is nog veel werk aan de winkel, maar we denken dat het vermogen om tegelijkertijd de levering van nanodeeltjes met hoge doorvoer en de cellulaire respons op nanodeeltjes uit te lezen, zal leiden tot betere mRNA-therapieën.”
Mede-hoofdauteur Paunovska zei dat zij en Dobrowolski op het idee kwamen voor het SENT-seq-systeem, “organisch, na twee maanden samenwerken”.
Dahlman voegde toe: “Ik ben trots op het werk dat Curtis, Kalina en het team in het lab hebben gedaan. Ik denk dat dit het begin is van een buitengewoon interessante fase in ons werk.”
Curtis Dobrowolski et al, Nanodeeltjes eencellige multiomische uitlezingen onthullen dat celheterogeniteit de door lipiden gemedieerde boodschapper-RNA-afgifte beïnvloedt, Natuur Nanotechnologie (2022). DOI: 10.1038/s41565-022-01146-9
Natuur Nanotechnologie
Geleverd door Georgia Institute of Technology