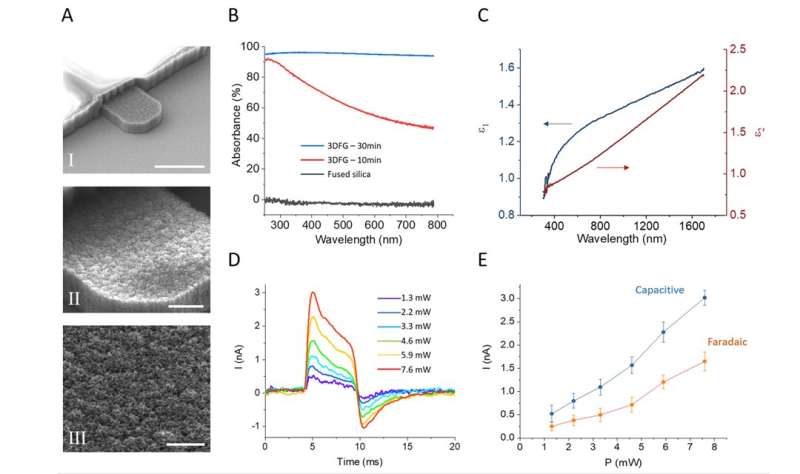
SEM-afbeeldingen geven een nadere blik op 3DFG-elektroden. Credit: Carnegie Mellon University, Afdeling Biomedische Technologie
Achter elke hartslag en elke hersensignaal zit een enorm orkest van elektrische activiteit. Hoewel de huidige elektrofysiologische observatietechnieken meestal beperkt zijn tot extracellulaire opnames, heeft een vooruitstrevende groep onderzoekers van de Carnegie Mellon University en Istituto Italiano di Tecnologia een flexibel, goedkoop en biocompatibel platform gevonden om rijkere intracellulaire opnames mogelijk te maken.
Het unieke “over de oceaan” -partnerschap van de groep begon twee jaar geleden op de Bioelectronics Winter School (BioEl) met plengoffers en een schets van een servet. Het is geëvolueerd tot onderzoek dat is gepubliceerd in Science Advances, waarin een nieuw micro-elektrodeplatform wordt beschreven dat gebruikmaakt van driedimensionaal vaag grafeen (3DFG) om rijkere intracellulaire opnames van cardiale actiepotentialen met een hoge signaal-ruisverhouding mogelijk te maken. Deze vooruitgang zou een revolutie teweeg kunnen brengen in het lopende onderzoek met betrekking tot neurodegeneratieve en hartaandoeningen, evenals de ontwikkeling van nieuwe therapeutische strategieën.
Een belangrijke leider in dit werk, Tzahi Cohen-Karni, universitair hoofddocent biomedische technologie en materiaalkunde en engineering, heeft gedurende zijn hele carrière de eigenschappen, effecten en mogelijke toepassingen van grafeen bestudeerd. Nu zet hij een gezamenlijke stap in een andere richting, met behulp van een verticaal gegroeide oriëntatie van het buitengewone op koolstof gebaseerde materiaal (3DFG) om toegang te krijgen tot het intracellulaire compartiment van de cel en intracellulaire elektrische activiteit vast te leggen.
Vanwege zijn unieke elektrische eigenschappen onderscheidt grafeen zich als een veelbelovende kandidaat voor op koolstof gebaseerde biosensoren. Recente studies hebben de succesvolle inzet van grafeenbiosensoren aangetoond voor het bewaken van de elektrische activiteit van cardiomyocyten, of hartcellen, buiten de cellen, of met andere woorden, extracellulaire opnames van actiepotentialen. Intracellulaire opnames zijn daarentegen beperkt gebleven vanwege ineffectieve hulpmiddelen… tot nu toe.
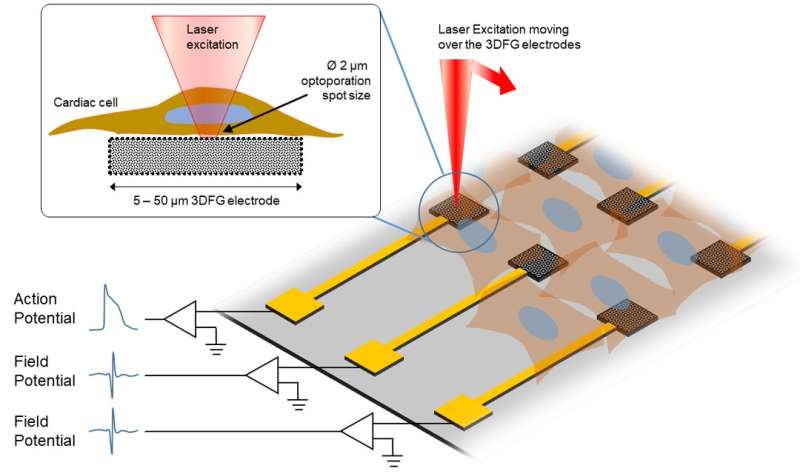
Deze schets toont de experimentele procedure van ultrasnelle laser die over de 3DFG-elektroden beweegt. Krediet: College of Engineering, Carnegie Mellon University
“Ons doel is om het hele orkest op te nemen – om alle ionenstromen te zien die het celmembraan passeren – niet alleen de subset van het orkest die wordt getoond door extracellulaire opnames”, legt Cohen-Karni uit. “Het toevoegen van de dynamische dimensie van intracellulaire opnames is fundamenteel belangrijk voor het screenen van geneesmiddelen en toxiciteitstesten, maar dit is slechts een belangrijk aspect van ons werk.”
“De rest is de technologische vooruitgang”, vervolgt Cohen-Karni. “3DFG is goedkoop, flexibel en een volledig koolstofplatform; er zijn geen metalen bij betrokken. We kunnen elektroden ter grootte van een wafel van dit materiaal genereren om binnen enkele seconden intracellulaire opnames op meerdere locaties mogelijk te maken, wat een aanzienlijke verbetering is ten opzichte van een bestaande tool, als een patchklem, die uren tijd en expertise vereist. “
Dus, hoe werkt het? Gebruikmakend van een techniek die is ontwikkeld door Michele Dipalo en Francesco De Angelis, onderzoekers van Istituto Italiano di Tecnologia, wordt een ultrasnelle laser gebruikt om toegang te krijgen tot het celmembraan. Door korte laserpulsen op de 3DFG-elektrode te laten schijnen, wordt een deel van het celmembraan op een bepaalde manier poreus, waardoor elektrische activiteit in de cel kan worden geregistreerd. Vervolgens worden de cardiomyocyten gekweekt om de interacties tussen de cellen verder te onderzoeken.
Interessant is dat 3DFG zwart is en het meeste licht absorbeert, wat resulteert in unieke optische eigenschappen. Gecombineerd met zijn schuimachtige structuur en enorme blootgestelde oppervlakte, heeft 3DFG veel wenselijke eigenschappen die nodig zijn om kleine biosensoren te maken.
“We hebben een slimmere elektrode ontwikkeld; een elektrode die ons een betere toegang geeft”, benadrukt Cohen-Karni. “Het grootste voordeel van mijn kant is dat we toegang hebben tot deze signaalrijkdom, om processen van intracellulair belang te kunnen onderzoeken. Het hebben van een dergelijk hulpmiddel zal een revolutie teweegbrengen in de manier waarop we effecten van therapeutica op terminale organen kunnen onderzoeken, zoals het hart.”
Naarmate dit werk vordert, is het team van plan zijn lessen toe te passen in grootschalige cel / weefsel-interfaces, om de weefselontwikkeling en toxiciteit van chemische verbindingen (bijv. Geneesmiddeltoxiciteit) beter te begrijpen.
Michele Dipalo et al. Intracellulaire actiepotentiaal opnames van cardiomyocyten door ultrasnelle gepulseerde laserbestraling van fuzzy grafeen micro-elektroden, Science Advances (2021). DOI: 10.1126 / sciadv.abd5175
Science Advances
Geleverd door Carnegie Mellon University, Department of Biomedical Engineering