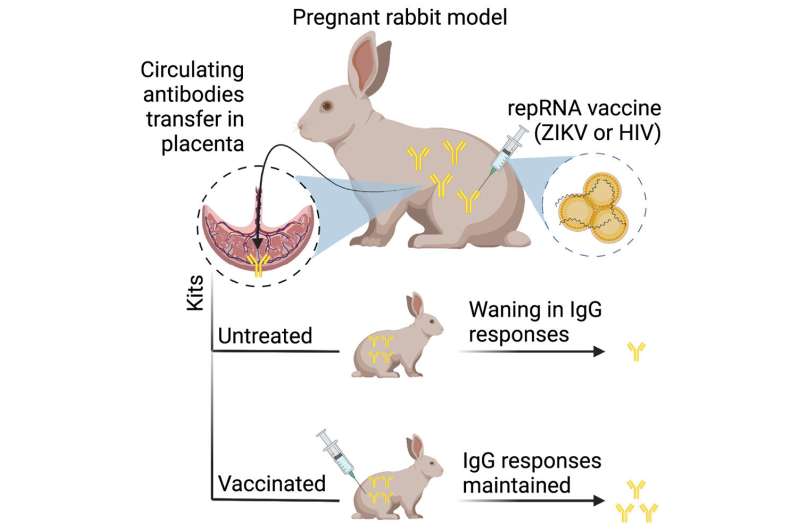
Grafisch abstract. Credit: Moleculaire therapie (2023). DOI: 10.1016/j.ymthe.2023.02.022
Nieuw ontwikkelde mRNA-vaccins tegen het Zika-virus en HIV-1 produceerden sterke antilichaamreacties die werden overgedragen van zwangere konijnen op hun nakomelingen, rapporteren onderzoekers in het tijdschrift Moleculaire therapie. Zoals opgemerkt door de auteurs, ondersteunen de resultaten de verdere ontwikkeling van hun vaccinplatform, LION/repRNA, voor maternale en neonatale omgevingen om te beschermen tegen de overdracht van ziekteverwekkers van moeder op kind bij dieren en mensen.
Het recente succes van mRNA-vaccins als reactie op de COVID-19-pandemie is een katalysator voor de ontwikkeling van mRNA-vaccins gericht op andere infectieziekten. De Amerikaanse Food and Drug Administration heeft toestemming gegeven voor mRNA-vaccins voor kinderen van 6 maanden en ouder, en voorlopige bevindingen bij zwangere vrouwen hebben geen duidelijke nadelige gevolgen aangetoond.
“Het voorkomen van overdracht van moeder op kind is een belangrijk doel voor het verminderen van de ziektelast bij pasgeborenen”, zegt senior auteur Amit Khandhar, een materiaalwetenschapper bij HDT Bio Corp. “Nu mRNA-vaccins wereldwijd de aandacht trekken, is het nodig om hun veiligheid te evalueren en immunogeniciteit in preklinische modellen die informatie geven over vaccinatie bij moeders en kinderen.”
Khandhar werkte samen met Herman Staats van Duke University School of Medicine en Noah Sather van Seattle Children’s Research Institute om zelfversterkende replicon (repRNA) vaccins te evalueren. De onderzoekers leverden de vaccins met hun formulering van LION-nanodeeltjes in de klinische fase af bij zwangere konijnen door het Zika-virus en HIV-1 als doelwitten voor ziektes te gebruiken. Deze twee ziekteverwekkers spelen een belangrijke rol bij het veroorzaken van infecties bij pasgeborenen na overdracht van moeder op kind.
De repRNA-vaccins coderen voor virale enzymen die de expressie van een van belang zijnd gen 10- tot 100-voudig versterken ten opzichte van niet-replicerend mRNA, wat doserings- en fabricagevoordelen oplevert.
De gepatenteerde LION-afgiftetechnologie is een stabiele olie-in-water-nanodeeltjesemulsie die nucleïnezuren elektrostatisch bindt en beschermt, in tegenstelling tot formuleringen van lipide-nanodeeltjes, die RNA inkapselen. Omdat LION onafhankelijk van repRNA wordt opgeslagen, heeft het plug-and-play-functionaliteit, waardoor nieuwe repRNA-vaccinconstructen snel kunnen worden geëvalueerd, zoals de constructen die recentelijk zijn ontwikkeld om opkomende SARS-CoV-2-varianten aan te pakken.
De resultaten toonden aan dat repRNA-immunisatie met een relatief hoge dosis goed werd verdragen en geen nadelige invloed had op de worpgrootte. De LION/repRNA-vaccins veroorzaakten ook robuuste antigeenspecifieke antilichaamresponsen bij volwassen zwangere konijnen die waarschijnlijk passief werden overgedragen op nakomelingen in de baarmoeder.
“Hoewel de sterke correlatie in zowel de omvang als de kwaliteit van antilichaamniveaus tussen moeders en pasgeborenen suggereert dat de antilichamen die in kits worden gedetecteerd waarschijnlijk passief van moeders zijn verkregen, kunnen we de mogelijkheid niet volledig uitsluiten dat het vaccin dat aan moeders wordt toegediend, zelf wordt verspreid naar kits. en actief antilichaamreacties opwekken, “zegt Khandhar.
De onderzoekers ontdekten ook dat de timing van maternale vaccinatie cruciaal was voor het maximaliseren van antilichaamoverdracht, en daaropvolgende vaccinatie bij pasgeborenen handhaafde verhoogde antilichaamniveaus in vergelijking met geen vaccinatie. Naast een geoptimaliseerde maternale vaccinatietiming kan actieve immunisatie bij pasgeborenen nodig zijn om de algehele antilichaamrespons bij zuigelingen na de geboorte te behouden. De auteurs zeggen dat er meer onderzoek nodig is om te bepalen of op RNA gebaseerde maternale vaccins bescherming kunnen bieden tegen infectie door overdracht van moeder op kind.
“De immunisatie-intervallen die we gebruikten, waren bijvoorbeeld niet geoptimaliseerd en zullen waarschijnlijk niet worden vertaald naar mensen vanwege verschillen in de draagtijd tussen konijnen en mensen”, zegt Khandhar. “Verdere studies zullen nodig zijn om boosting-intervallen en de duurzaamheid van antilichaamresponsen te testen om passieve antilichaamoverdracht naar pasgeborenen te maximaliseren. Ten slotte zullen aanvullende studies nodig zijn die zijn ontworpen om veiligheidssignalen in maternale en neonatale modellen te meten, alvorens door te gaan naar klinische evaluatie.”
Meer informatie:
Amit P. Khandhar et al., Evaluatie van repRNA-vaccin voor inductie en in utero overdracht van maternale antilichamen in een zwanger konijnenmodel, Moleculaire therapie (2023). DOI: 10.1016/j.ymthe.2023.02.022
Tijdschrift informatie:
Moleculaire therapie
Aangeboden door Cell Press