De intracellulaire detectierobot voert automatisch kwantitatieve metingen uit op meerdere cellen. Krediet: Weikang Hu, Zuidelijke Universiteit voor Wetenschap en Technologie
Een onderzoeksteam van de Southern University of Science and Technology ontwikkelde een geautomatiseerd intracellulair detectiesysteem, dat een zeer efficiënte benadering biedt om cellulaire intrinsieke kenmerken en heterogeniteit te onthullen voor een beter onderzoek naar ziekteprogressie of vroege diagnose van de ziekte. De nieuwe onderzoekspaper werd op 2 september gepubliceerd in het tijdschrift Cyborg en bionische systemen.
Meting van intracellulaire biochemische processen is belangrijk om de functie van biologische systemen kwantitatief te begrijpen. Op nanopipetten gebaseerde intracellulaire detectie is een in-situ, labelvrije en niet-destructieve meetmethode. De kleine omvang van cellen en de tip van de nanopipet maken het echter moeilijk om intracellulaire metingen efficiënt uit te voeren door handmatige manipulatie, wat een hindernis vormt bij het verkrijgen van statistisch significante gegevens. Daarom ontwierpen onderzoekers een zeer efficiënt en consistent intracellulair detectiesysteem door automatiseringstechnologie te integreren.
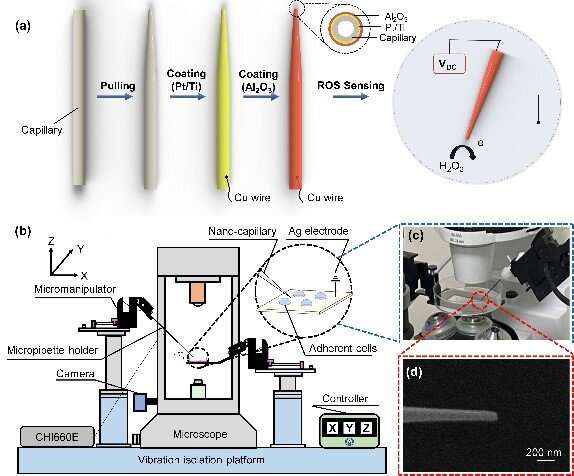
Eerst werd de op nanopipet gebaseerde sensor met een tipdiameter van ongeveer 100 nm ontworpen, waarbij een platinaring op de nanopipettip werd gebruikt als een werkelektrode voor de elektrochemische detectie van reactieve zuurstofsoorten (ROS). Tegelijkertijd werd de sensor gemonteerd op een zeer nauwkeurige micromanipulator met een bewegingsresolutie van 5 nm en werd een omgekeerde fluorescentiemicroscoop gebruikt voor visuele feedback.
Bovendien stelde het team een labelvrij celdetectie-algoritme voor, dat de invloed van fluorescerende kleuring op cellen kan vermijden en de penetratieplaatsen nauwkeurig kan lokaliseren voor zeer efficiënte intracellulaire meting. Het algoritme verplaatst de cellen automatisch naar een defocusvlak om het grijsschaalverschil tussen de aanhangende cellen en de achtergrond te maximaliseren, waardoor de celdetectie wordt vereenvoudigd en de celherkenningssnelheid wordt verbeterd.
Bovendien werd een non-overshoot nanopipetpuntpositionering ontwikkeld om de tipschade te voorkomen die wordt veroorzaakt door de tip die tijdens autofocus tegen de celschotel botst. In het bijzonder werden de genormaliseerde correlatiecoëfficiënten tijdens het matchen van sjablonen op verschillende z-asposities gebruikt als de focusmaat om de nanopipetpunt automatisch te focussen zonder doorschieten en tipschade.
Bovendien werd nabijheidsdetectie op basis van ionenstroomfeedback gebruikt om de relatieve hoogte tussen de nanopipettip en het celoppervlak nauwkeurig te bepalen vanwege de zeer gevarieerde dikte van de hechtende cellen. Wanneer de nanopipettip de cel nadert, wordt de tip geleidelijk geblokkeerd door de cel en zal de ionenstroom door de tipopening afnemen. Daarom kan de relatieve hoogte tussen de punt en de cel nauwkeurig worden gemeten.
Ten slotte werden de celpenetratie en elektrochemische detectie van ROS geëvalueerd door menselijke borstkankercellen en zebravisembryocellen, en de variatie van ROS-signalen geeft aan dat het systeem in staat is tot een zeer selectieve respons op ROS en kwantitatieve meting van intracellulaire ROS.
Dit werk biedt een systematische aanpak voor geautomatiseerde intracellulaire detectie van hechtende cellen, waarmee een solide basis wordt gelegd voor detectie, diagnose en classificatie van verschillende vormen van biochemische reacties binnen afzonderlijke cellen met hoge doorvoer. Bovendien zal het voorgestelde systeem ook belangrijke toepassingen hebben in het traceren van afstammingslijnen voor ontwikkelingsbiologie en manipulatie met hoge resolutie van organellen in levende afzonderlijke cellen voor het onderzoeken van de specifieke oorzaken van ziekten en de ontwikkeling van nieuwe therapieën.
Het artikel, “Robotic Intracellular Electrochemical Sensing for Adherent Cells”, werd gepubliceerd in het tijdschrift Cyborg en bionische systemen op 2 september 2022.
Weikang Hu et al, Robotic intracellulaire elektrochemische detectie voor hechtende cellen, Cyborg en bionische systemen (2022). DOI: 10.34133/2022/9763420
Geleverd door Beijing Institute of Technology Press