Maar wetenschappers zeggen dat het aanbrengen van veranderingen in het DNA die kunnen worden doorgegeven, nog niet veilig en effectief is

In 2018 kondigde Jiankui He (foto) aan dat hij genen in embryo’s had bewerkt om twee babymeisjes te creëren, in strijd met de algemene consensus dat de technologie niet klaar is voor een dergelijke stap.
Het bewerken van genen om erfelijke veranderingen in het menselijk DNA aan te brengen is nog niet veilig en effectief genoeg om genetisch gemodificeerde baby’s te maken, zegt een internationale wetenschappelijke commissie. Maar in een rapport van 3 september legde de groep een routekaart uit voor het uitrollen van erfelijke genbewerking, mocht de samenleving besluiten dat dit soort DNA-wijziging acceptabel is.
De International Commission on the Clinical Use of Human Germline Genome Editing werd opgericht nadat een Chinese wetenschapper in 2018 aankondigde dat hij twee gen-bewerkte babymeisjes had gemaakt, wat tot verontwaardiging leidde (SN: 27-11-18). In de eerste officiële afweging over de kwestie, de groep bevat strikte wetenschappelijke criteria waaraan moet worden voldaan voordat erfelijke genbewerking klinisch kan worden geprobeerd. Als landen er niet voor kunnen zorgen dat aan al deze criteria wordt voldaan, mag erfelijke genbewerking niet worden goedgekeurd, zeggen de commissarissen.
Toch beweren sommige critici dat zelfs het presenteren van dergelijke criteria voorbarig is. De wetenschap zou moeten wachten tot de samenleving beslist of genbewerking toegestaan is die toekomstige generaties kan beïnvloeden, zeggen ze.
Genbewerking omvat het veranderen van een enkele DNA-letter of -basis in een gen. Veel verschillende technologieën, waaronder CRISPR / Cas9, basiseditors (SN: 3/5/19) en gemanipuleerde eiwitten genaamd zinkvingernucleasen en TALEN’s (SN: 6-11-15), kan worden gebruikt om bewerkingen uit te voeren op precieze locaties in het DNA. Hoewel de nauwkeurigheid van het bewerken is verbeterd, zijn er nog steeds zorgen dat geneditors ongewenste, “off-target” veranderingen elders in het DNA zullen aanbrengen die schade kunnen veroorzaken. Technologieën om ervoor te zorgen dat elke cel in een embryo de gewenste verandering – en alleen die verandering – bevat, hebben ook nog werk nodig, zegt de commissie.
“Het is nauwkeurig en efficiënt genoeg om te doen bij dieren”, maar het bewerken van menselijke embryo’s vereist veel meer precisie, zei Haoyi Wang, een geneticus en moleculaire en stamcelbioloog aan het Institute of Zoology van de Chinese Academy of Sciences in Beijing, op 3 september tijdens een webinar om het rapport te bespreken.
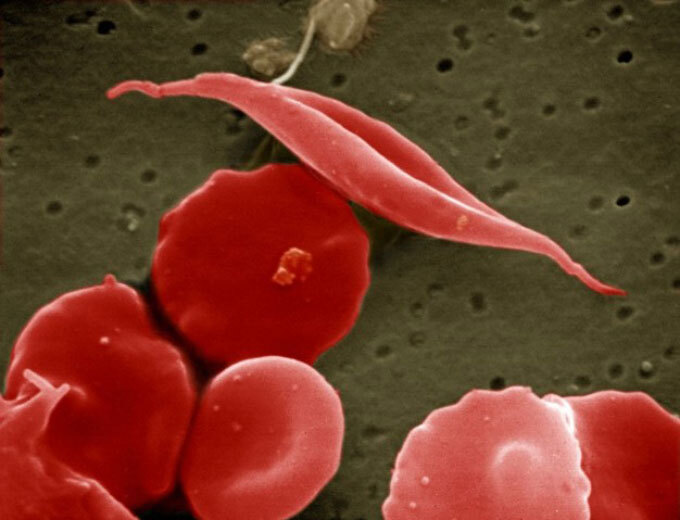
Wetenschappers testen CRISPR-genbewerking al om de erfelijke bloedaandoeningen sikkelcelanemie en bèta-thalassemie en een erfelijke vorm van blindheid genaamd Leber congenitale amaurosis 10 bij volwassenen te corrigeren (SN: 14-8-19). Die bewerkingen bevinden zich in cellen voor volwassenen en kunnen niet worden overgedragen naar toekomstige generaties.
Maar het veranderen van DNA in de menselijke kiembaan – embryo’s, eieren, sperma of de cellen waaruit ze voortkomen – zou veranderingen creëren die kunnen worden doorgegeven aan toekomstige generaties. Veel mensen, waaronder wetenschappers, zijn bezorgd dat malafide wetenschappers niet zouden stoppen bij het uitzoeken van ziektes en ‘designerbaby’s’ zouden creëren met verbeterde atletische vaardigheden, intelligentie of andere wenselijke eigenschappen.
De commissie stelt voor om het bewerken van de menselijke kiembaan te beperken tot ernstige genetische ziekten die worden veroorzaakt door specifieke versies van enkele genen die vrijwel gegarandeerd de ziekte veroorzaken als ze worden overgeërfd. Dergelijke aandoeningen omvatten spierdystrofie van Duchenne, de ziekte van Tay-Sachs en cystische fibrose. Kinderen die deze aandoeningen erven, sterven jong of hebben ernstige medische problemen.
De commissie specificeerde ook dat voordat de menselijke kiembaanbewerking wordt overwogen, er geen andere manier beschikbaar zou moeten zijn om ervoor te zorgen dat een paar embryo’s kan produceren zonder de ziekteverwekkende genetische varianten. Dat leidt in essentie tot paren waarin beide ouders twee exemplaren hebben van recessieve ziekteverwekkende varianten, of paren waarin één ouder twee exemplaren heeft van mutaties die een dominante genetische aandoening veroorzaken, zoals de ziekte van Huntington, die het gevolg is van overerving. een enkele kopie van een defect gen.
Misschien zouden twintig families over de hele wereld aan deze strikte criteria voldoen, zei Michèle Ramsay, een menselijke geneticus aan de Universiteit van de Witwatersrand in Johannesburg, op 3 september tijdens een nieuwsbriefing.
Daarom besloot de commissie ook dat sommige gezinnen met minder ernstige aandoeningen, maar die weinig kans hebben om embryo’s te produceren zonder de ziekteverwekkende varianten, ook in aanmerking zouden komen. Een voorbeeld is familiaire hypercholesterolemie, een erfelijke vorm van hoog cholesterol die leidt tot vroege hartziekte en overlijden. Die en andere aandoeningen worden gedragen door een groot deel van de mensen in delen van de wereld waar huwelijken tussen neven en nichten veel voorkomen. Het bewerken van genen zou een optie kunnen zijn als 25 procent of minder van de embryo’s van een paar vrij zou zijn van de ziekteverwekkende mutatie.
Zelfs dan moeten dergelijke paren al in-vitrofertilisatie hebben geprobeerd met een techniek die pre-implantatie genetische testen wordt genoemd om embryo’s te screenen die de defecte versie van het gen dragen. “We denken niet dat er veel mensen zullen zijn” die gekwalificeerd zijn om deel te nemen aan het eerste onderzoek, zei Ramsay. “Er zullen geen sluizen worden geopend.” Als de technologie zowel veilig als effectief is in die paar gezinnen, kan deze worden overwogen voor andere aandoeningen.
De commissie beveelt aan om meer onderzoek te doen naar het gebruik van stamcellen voor de productie van eieren en sperma in laboratoriumschaaltjes, die vervolgens kunnen worden gebruikt om embryo’s te creëren die geen genetische ziekten dragen. Dergelijk onderzoek is gedaan bij muizen (SN: 18-5-17), maar staat nog in de kinderschoenen met menselijke cellen, zei Richard Lifton, een menselijke geneticus aan de Rockefeller University in New York City.
Overmoed afwenden was een van de belangrijkste zorgen van de commissie, zei Lifton. Het rapport beveelt ook aan om een internationale wetenschappelijke adviesraad op te richten om de stand van de technologie te evalueren en om te raadplegen over toepassingen om dergelijke erfelijke of kiembaanbewerkingen uit te voeren.
Een organisatie vergelijkbaar met het World Anti-Doping Agency, die toezicht houdt op het gebruik van prestatiebevorderende medicijnen in de sport, zou kunnen worden opgericht om op te letten voor ongeautoriseerde genbewerking, stelde Lifton voor. Het beteugelen van malafide wetenschappers zou ook het opzetten van een manier vereisen waarop klokkenluiders mogelijk niet-goedgekeurd onderzoek kunnen melden.
Het rapport is “behoorlijk voorzichtig en attent en geschreven met een duidelijke waardering voor wat er in de wereld gebeurt”, zei Kyle Orwig, een onvruchtbaarheidsonderzoeker aan de Universiteit van Pittsburgh die niet betrokken was bij de commissie. “Het is een beetje ambitieus omdat het vragen oproept over de vraag of individuele landen bereid zijn zich aan internationaal toezicht te onderwerpen”, voegde hij eraan toe.
Bovendien is het opzetten van mondiaal bestuur om te voorkomen dat wetenschappers schurken gaan gebruiken misschien niet zo effectief als het instellen van een duidelijk moratorium of verbod, zegt Katie Hasson, programmadirecteur voor genetische rechtvaardigheid bij het non-profit Centre for Genetics and Society, gevestigd in Berkeley, Californië. .
Of wijzigingen in het DNA worden toegestaan die kunnen worden geërfd door toekomstige generaties, is een beslissing die de hele menselijke soort raakt, en zou een internationale consensus moeten zijn in plaats van een beslissing van een enkel land, zei Wang.
Dit rapport behandelde alleen de wetenschappelijke aspecten van genbewerking. Een volgend rapport van de Wereldgezondheidsorganisatie zal ethische en maatschappelijke kwesties rond genbewerking aanpakken.
Het is achterlijk om uit te zoeken hoe je kiembaanbewerking moet doen voordat de samenleving heeft aangegeven dat te willen, zegt Hasson. “De vraag was en is nog steeds of we verder willen gaan met het bewerken van de genen en eigenschappen van toekomstige generaties”, zegt ze. ‘Om verder te gaan met hoe. . . lijkt een beetje op de zaken vooruit te lopen. “
Er is nog steeds behoefte aan brede maatschappelijke gesprekken over de technologie. Meer dan 70 landen hebben al wetten die het bewerken van kiembaanlijnen verbieden, en een moratorium en andere wetten kunnen de vooruitgang van de technologie effectief tegenhouden, zegt Hasson. ‘Er is geen reden waarom dit onvermijdelijk zou zijn. Door dit pad van tevoren uit te stippelen, lijkt het onvermijdelijker en worden we naar die conclusie gestuwd. “