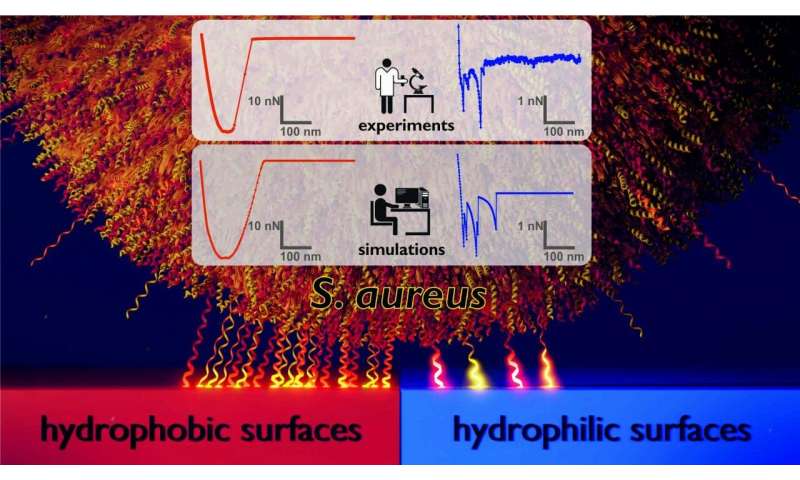
Model van het adhesiemechanisme waarmee de bacterie Staphylococcus aureus zich bindt aan hydrofobe (‘low-energy’) oppervlakken (links) vergeleken met hydrofiele (‘high-energy’) oppervlakken (rechts). Aan de linkerkant is een groot aantal celwandmoleculen (hier weergegeven als kleine samendrukbare veren) betrokken bij het binden van de cel aan het hydrofobe oppervlak. Op het hydrofiele oppervlak hiernaast zijn veel minder moleculen betrokken. De resultaten werden verkregen door een team van experimentele en theoretische natuurkundigen aan de Saarland University die computationele Monte Carlo-simulaties uitvoerden van kracht-afstandgegevens van atomaire krachtmicroscopie-experimenten. Krediet: Saarland University
Resultaten van studies in zowel experimentele als theoretische fysica kunnen helpen om antibacteriële oppervlakken te verbeteren. Het onderzoekswerk is onlangs gepubliceerd in het tijdschrift Nanoschaal.
Staphylococcus aureus bacteriën zijn een van de meest voorkomende oorzaken van infecties die patiënten oplopen tijdens een ziekenhuisopname. Deze ziekteverwekkers zijn bijzonder problematisch omdat ze robuuste biofilms kunnen vormen op zowel natuurlijke als kunstmatige oppervlakken waarvan ze zeer moeilijk te verwijderen zijn. “De individuele bacteriën in deze biofilms worden effectief beschermd tegen aanvallen door antibiotica of door het menselijk immuunsysteem. Daarom kan het zo gevaarlijk zijn wanneer deze bacteriën medische implantaten koloniseren, omdat ze dan ernstige postoperatieve infecties kunnen veroorzaken”, legt Karin Jacobs uit. Hoogleraar experimentele fysica aan de universiteit van Saarland. Het is daarom cruciaal om te proberen de vorming van deze biofilms te voorkomen.
Om de biofilmgroei te kunnen beïnvloeden, moesten de onderzoekers echter de mechanismen begrijpen waarmee de bacteriën zich aan verschillende materialen hechten. Met behulp van een scanning-atomaire-krachtmicroscoop drukten ze de minuscule bacteriecellen op verschillende soorten oppervlakken en bepaalden vervolgens de kracht die nodig was om de gehechte cellen van het oppervlak te tillen. Deze experimentele configuratie stelde de onderzoekers in staat om zogenaamde kracht-afstandcurves vast te leggen. “We gebruikten extreem gladde siliciumoppervlakken als modeloppervlakken. In de ene reeks experimenten werden de siliciumoppervlakken zo geprepareerd dat ze een hoge bevochtigbaarheid met water hadden; in een andere reeks experimenten werden ze behandeld als zeer hydrofoob. We konden dat aantonen. de bacteriecellen hechten veel sterker aan de hydrofobe oppervlakken, waarvan het water gewoon wegrolde, dan aan de hydrofiele (met water bevochtigbare) oppervlakken ”, legt Karin Jacobs uit.
Maar niet alleen de grootte van de krachten verschilt tussen de twee oppervlaktetypes, maar ook de vormen van de kracht-afstandcurves (zie figuur). “Op de hydrofobe oppervlakken zien we zeer gladde curven met een karakteristieke komvorm. Op de hydrofiele oppervlakken daarentegen zien we kracht-afstand curven met een zeer grillig profiel”, zegt professor Jacobs.
Om deze resultaten te begrijpen, werd de dynamica van deze complexe systemen gemodelleerd met behulp van Monte Carlo-simulaties die werden uitgevoerd in de onderzoeksgroep onder leiding van professor Ludger Santen, hoogleraar theoretische fysica aan de Saarland University. Het model behandelt de bacteriecel als een starre bol en de moleculen in de celwand die de cel aan de oppervlakte binden als minuscule veertjes. “Het blijkt dat om de experimentele resultaten te reproduceren, de rol die wordt gespeeld door de willekeurige (stochastische) aard van het moleculaire bindingsproces belangrijker is dan het proberen om de complexiteit van het model te vergroten. We hebben nu ontdekt waarom de bacteriecellen zich gedragen. zo anders op verschillende soorten oppervlakken. Op hydrofobe oppervlakken hecht een groot aantal celwandeiwitten zich aan het oppervlak, wat resulteert in een sterke bindingskracht en een vloeiende kracht-afstand curve, ”legt Ludger Santen uit.
Daarentegen zijn op een hydrofiel oppervlak veel minder celwandeiwitten betrokken bij het vastbinden van de bacterie aan het oppervlak. Hierdoor worden de bacteriën minder sterk aan het oppervlak vastgehouden en is de vorm van de kracht-afstand curve minder uniform. “De grillige vorm van de rondingen die we zien bij hydrofiele oppervlakken wordt veroorzaakt door een paar individuele celwandmoleculen die van het oppervlak worden getrokken. Omdat er minder celwandeiwitten bij betrokken zijn, binden de bacteriën zich minder sterk aan hydrofiele oppervlakken”, zegt Erik Maikranz, die de Monte Carlo-simulaties uitvoerde als onderdeel van zijn promotieonderzoek.
Door de verschillende vormen van de kracht-afstandcurven veronderstellen de natuurkundigen dat op een hydrofiel oppervlak minder celwandproteïnen betrokken zijn bij het bindingsproces omdat deze moleculen eerst een potentiaalbarrière moeten overwinnen, waardoor het aantal proteïnemacromoleculen dat effectief wordt verminderd kan de cel aan de oppervlakte vastmaken. “De potentiële barrière voor adhesie op hydrofiele oppervlakken is relatief hoog, dus slechts enkele celwandproteïnen zijn in staat om deze energiebarrière in een bepaalde tijd te overwinnen. Op hydrofobe oppervlakken is de barrière echter verwaarloosbaar klein, zodat muureiwitten kunnen direct aan het oppervlak hechten ”, legt dr. Christian Spengler uit, die de experimenten in het onderzoek uitvoerde.
Erik Maikranz et al, Verschillende bindingsmechanismen van Staphylococcus aureus aan hydrofobe en hydrofiele oppervlakken, Nanoschaal (2020). DOI: 10.1039 / d0nr03134h
Nanoschaal
Geleverd door Saarland University