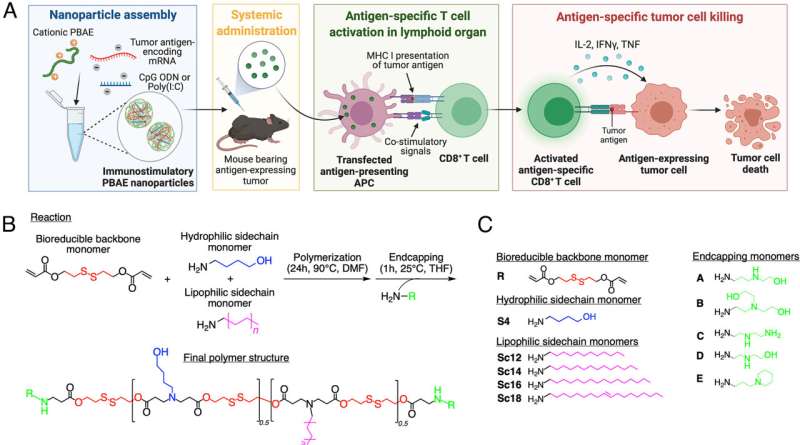
Bioreduceerbare lipofiele PBAE-mRNA-nanodeeltjes (NP’s) als kankervaccin. (A) Schema van de op mRNA gebaseerde kankervaccintechnologie met behulp van polymere (PBAE) NP’s. (B) Reactieschema voor bioreduceerbare lipofiele PBAE’s. Het biologisch reduceerbare monomeer van de diacrylaathoofdketen (R) wordt gepolymeriseerd met een 1:1-mengsel van een hydrofiel aminezijketenmonomeer (S4) en een lipofiel aminezijketenmonomeer (Sc12-18) via Michael-additie. Het verkregen willekeurige copolymeer met diacrylaat-eindgroepen wordt afgesloten met een aminebevattend monomeer (A-E) om de uiteindelijke polymeerstructuur te vormen. (C) Monomeren gebruikt in de combinatorische bibliotheeksynthese om bioreduceerbare lipofiele PBAE’s te vormen. Credit: Procedures van de National Academy of Sciences (2023). DOI: 10.1073/pnas.2301606120
Wetenschappers van Johns Hopkins Medicine zeggen dat ze een nanodeeltje hebben ontwikkeld – een extreem kleine biologisch afbreekbare container – die het potentieel heeft om de levering van op boodschapperribonucleïnezuur (mRNA) gebaseerde vaccins voor infectieziekten zoals COVID-19 te verbeteren, en vaccins voor de behandeling van niet- infectieziekten waaronder kanker.
Resultaten van tests bij muizen, gerapporteerd op 20 juni in de Procedures van de National Academy of Scienceslaten zien dat het afbreekbare, op polymeer gebaseerde nanodeeltje dat een op mRNA gebaseerd vaccin draagt, na injectie in de bloedbaan van muizen, in staat was om naar de milt te reizen en bepaalde kankerbestrijdende immuuncellen op een gerichte manier te activeren.
De onderzoekers ontdekten ook dat muizen met melanoom twee keer zo lang overleefden, en tweemaal het aantal muizen met colorectale kanker overleefde op lange termijn, na een injectie van de door Johns Hopkins gemaakte nanodeeltjes in vergelijking met muizen die controlebehandelingen kregen.
Bovendien ontdekten de wetenschappers dat in alle muizen ongeveer de helft van de gespecialiseerde immuuncellen die verantwoordelijk zijn voor het herkennen en vernietigen van ongezonde cellen, zoals cellen die zijn geïnfecteerd met virussen of kanker, was geactiveerd en voorbereid om de specifieke binnendringende kankercellen te herkennen.
Nanodeeltjes gemaakt van lipiden (een soort vetzuur) vormen de basis voor mRNA COVID-19-vaccins. Dergelijke op lipiden gebaseerde, preventieve vaccins worden meestal in de spieren geïnjecteerd.
Hoewel spieren veel cellen bevatten die in staat zijn om mRNA tot expressie te brengen dat kan leiden tot een antilichaamrespons, zijn er relatief weinig dendritische cellen – immuuncellen die de rest van het immuunsysteem, in het bijzonder T-cellen, leren om kankercellen op te sporen en te vernietigen. Wetenschappers kunnen mogelijk op kankerbehandeling gerichte vaccins verbeteren door hun vermogen om dendritische cellen te bereiken met hun mRNA-instructies te vergroten.
Het injecteren van op lipiden gebaseerde vaccins in de bloedbaan is moeilijk gebleken omdat de vaccins de neiging hebben rechtstreeks naar de lever te reizen, waar ze worden afgebroken.
“Ons doel was om een nanodeeltje te ontwikkelen dat niet rechtstreeks naar de lever zou worden gestuurd en dat cellen van het immuunsysteem effectief zou kunnen leren om het juiste doelwit te zoeken en te vernietigen”, zegt Jordan Green, Ph.D., professor biomedische technologie aan de Johns Hopkins University School of Medicine.
Green legt uit dat om sterkere vaccins te maken voor infectieziekten en voor niet-infectieuze ziekten, zoals kanker, de mRNA-inhoud van het nanodeeltje nodig is om de dendritische cellen te bereiken, binnen te gaan en tot expressie te worden gebracht. Nadat het mRNA tot expressie is gebracht in dendritische cellen, wordt het snel afgebroken, en de resulterende reactie van de immuuncel kan veel langer aanhouden nadat het mRNA en de nanodeeltjes allang verdwenen zijn, zeggen de onderzoekers.
Gewoonlijk hebben wetenschappers deze celtargeting tot stand gebracht door eiwitten aan een nanodeeltje te hechten die zich specifiek, zoals een slot en een sleutel, binden aan het oppervlak van een doelcel. In laboratoriumtests van deze aanpak bereikt echter slechts een klein percentage van de nanodeeltjes de doelcel, en de wetenschappers zeggen dat er productie-uitdagingen zijn met dergelijke benaderingen.
Green en zijn team testten verschillende materialen en besloten uiteindelijk om een gewenst mRNA in een op polymeer gebaseerd vat te plaatsen. Polymeren zijn repetitieve groepen van kleine moleculen die een hecht gebonden keten vormen om een groter molecuul te creëren, en ze kunnen zo worden ontworpen dat ze biologisch worden afgebroken tot kleine moleculen in het lichaam. Het team van Green ontwikkelde de verhouding van het nanodeeltje van waterminnende tot waterfobe moleculen precies goed – een sleutel om het nanodeeltje geschikter te maken om mRNA in te kapselen en het gemakkelijker te maken om de doelcel binnen te gaan.
Vervolgens gebruikte het team van Green disulfidebindingen om de nanodeeltjes snel in de doelcel af te breken. De polymeren die werden gebruikt om de nanodeeltjes te construeren, bevatten eindafsluitende moleculen die affiniteit hebben voor een specifiek weefseltype.
Ten slotte voegden Green en zijn team een ”helper”, ook wel een adjuvans genoemd, toe aan het nanodeeltje. Het adjuvans helpt de dendritische cel te activeren.
In experimenten met cellen die in het laboratorium waren gekweekt, ontdekten de onderzoekers dat de nanodeeltjesconfiguratie die ze ontwikkelden, werd overgenomen door primaire dendritische cellen op niveaus die ongeveer vijftig keer hoger waren dan mRNA alleen. Bij muizen waren bijna 80% van de cellen in de milt die de nanodeeltjes bereikten, de beoogde dendritische cellen.
In een reeks experimenten gebruikten de onderzoekers muizen met immuuncellen die genetisch gemanipuleerd waren om rood te gloeien als het nanodeeltje werd geopend om de mRNA-inhoud te onthullen. Ze ontdekten dat 5% tot 6% van alle dendritische cellen in de milt het nanodeeltje met succes opnam, opende en verwerkte, en dat dit vooral gebeurde in dendritische cellen in vergelijking met andere immuuncellen, waaronder macrofagen, monocyten, neutrofielen en T-cellen.
“Het immuunsysteem is ontworpen om door een versterkte reactie te werken, waarbij dendritische cellen andere immuuncellen leren waarnaar ze in het lichaam moeten zoeken”, zegt Green.
Latere experimenten toonden aan dat de helft van de muizen met darmkanker langdurig overleefde na twee injecties van de nieuwe nanodeeltjesformulering plus een immunotherapie-medicijn, vergeleken met 10% tot 30% die overleefden na behandeling met andere nanodeeltjesformuleringen en een immunotherapie-medicijn of de immunotherapie. medicijn alleen.
Van de langdurig overlevende muizen met colorectale kanker leefden ze allemaal zonder aanvullende behandeling toen de onderzoekers hen extra colorectale kankercellen gaven, wat duidt op een langdurige immunologische respons die verhinderde dat de kanker terugkeerde.
De onderzoekers ontdekten ook dat 21 dagen na de behandeling met het nieuwe nanodeeltje, 60% van de celdodende T-cellen in de muizen gewapend waren om de colorectale cellen te herkennen en aan te vallen. Evenzo was bij muizen met melanoom ongeveer de helft van hetzelfde type T-cellen voorbereid om melanoom aan te vallen.
“Het systeem voor het afleveren van nanodeeltjes was in staat om een leger van T-cellen te creëren die aan kanker gekoppelde antigeen kunnen herkennen”, zegt Green.
“Dit nieuwe toedieningssysteem voor nanodeeltjes kan de manier verbeteren waarop vaccins worden gegeven voor infectieziekten, en het kan ook een nieuwe weg openen voor de behandeling van kanker”, zegt Green.
Meer informatie:
Elana Ben-Akiva et al, Biologisch afbreekbare lipofiele polymere mRNA-nanodeeltjes voor ligandvrije targeting van milt-dendritische cellen voor kankervaccinatie, Procedures van de National Academy of Sciences (2023). DOI: 10.1073/pnas.2301606120
Tijdschrift informatie:
Procedures van de National Academy of Sciences
Geleverd door de Johns Hopkins University School of Medicine