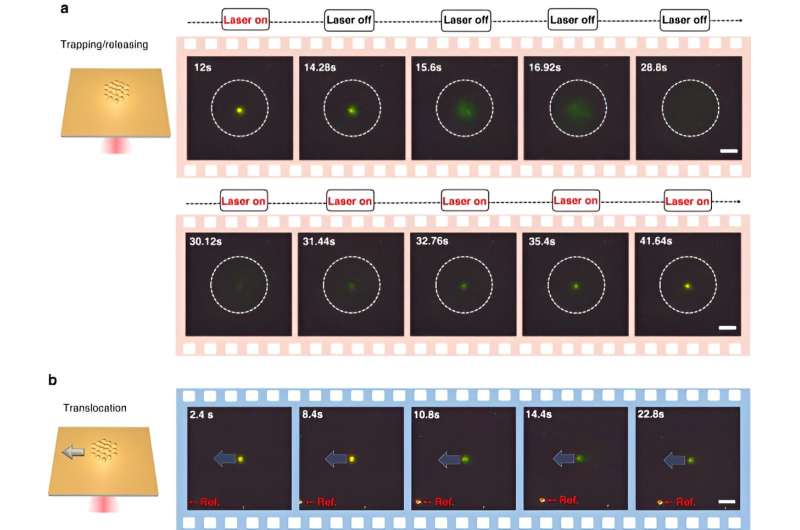
Opeenvolgende microscoopframes tonen het proces van insluiting, vrijgave en translocatie van goudnanodeeltjes. a Een frame-voor-frame sequentie van het vangen en vrijgeven van DNA@AuNS, de gestippelde cirkel geeft het vanggebied aan. b Een frame-voor-frame sequentie van de translocatie van een cluster van gevangen DNA@AuNSs. Het laservermogen is 0,33 mW, de AuNS- en PEG-concentratie zijn respectievelijk 100 μM en 10% (gew%). Scalerbalk = 4 μm. Credit: Licht: Wetenschap en toepassingen, doi: 10.1038/s41377-023-01326-9
Optothermische nanopincetten zijn een innovatieve optische ontwerpmethode die een revolutie teweeg heeft gebracht in klassieke optische technieken om een breed scala aan nanodeeltjes te vangen. Hoewel het optothermische temperatuurveld kan worden gebruikt voor in situ regulering van nanodeeltjes, blijven er uitdagingen bestaan bij het identificeren van hun potentieel voor het reguleren van bionanodeeltjes.
Om de synergetische effecten van optothermische manipulatie en op Clustered Regularly Interspaced Short Palindromic Repeats (CRISPR) gebaseerde biodetectie te observeren, ontwikkelden de onderzoekers een combinatie van CRISPR-aangedreven optothermische nanopincetten, afgekort als CRONT.
In een nieuw rapport in Licht: wetenschap en toepassingenbereikten Jiajie Chen en een onderzoeksteam op het gebied van opto-elektronica, biomedische technologie en natuurkunde dit door gebruik te maken van diffusieforese En thermo-osmotische stromen voor optothermale excitatie door het succesvol verrijken van DNA-gefunctionaliseerde gouden nanodeeltjes, CRISPR-geassocieerde eiwitten en DNA-strengen.
De wetenschappers bouwden voort op een optothermisch schema om CRISPR-geassocieerde detectie van single-nucleotide polymorfisme op het niveau van één molecuul te verbeteren, om een nieuwe op CRISPR gebaseerde methode te introduceren om nucleotide-splitsing te observeren. De onderzoekers bestudeerden deze innovatieve aanpak als universele point-of-care-diagnostiek, biofotonicaEn bionanotechnologie veld.
Optische pincet
In 1986, Arthur Ashkin heeft het optische pincet uitgevonden om nano-objecten op afstand te reguleren en ontving in 2018 een Nobelprijs voor de natuurkunde voor deze baanbrekende ontdekking en bijdrage aan biologische systemen. Terwijl klassieke optische pincetten afhankelijk zijn van de momentumtransformatie van licht, komen interdisciplinaire combinaties voor plasmonische optica, elektrisch veld En temperatuur hebben de grenzen effectief aangepakt.
Er is een verscheidenheid aan innovatieve benaderingen ontstaan die nieuwe mogelijkheden bieden op het gebied van deeltjesanalyse en -regulering. Optothermische nanopincetten gebruiken optisch geïnduceerde thermodynamische krachten om nanodeeltjes op micronschaal te reguleren sub-micron precisie.
In vergelijking met traditionele optische pincetten vereisen optothermische pincetten een lagere vermogensdichtheid, waardoor ze een aantrekkelijk alternatief zijn voor biologische detectie, terwijl de nadelige optische effecten op biologische monsters worden verminderd. Omdat thermische effecten een sleutelrol spelen tijdens een verscheidenheid aan biologische processen, is het mogelijk om de mogelijkheden van het temperatuurveld te benutten voor praktische toepassingen.
De methode kan worden gebruikt om bionanodeeltjes te reguleren, variërend van micro- tot nanoschaal, inclusief bacteriën en levende cellen, evenals enkel- en dubbelstrengige DNA-moleculen en eiwitten.
CRISPR combineren met nanopincetten: CRONT
Het geclusterde CRISPR-systeem (Regelly Interspaced Short Palindrome Repeat) biedt zelf een opmerkelijk hulpmiddel voor het bewerken van genen, dat ook een Nobelprijs in 2020. De methode omvatte een CRISPR-geassocieerd nuclease-eiwit en een doel-DNA-specifiek gids-RNA.
Biofysici en bio-ingenieurs willen steeds meer de gevoeligheid en veelzijdigheid van DNA-detectie vergroten door het CRISPR-Cas-systeem te combineren met nieuwe detectiemodi.
Om de bestaande beperkingen van de methode te overwinnen, ontwierpen Chen en collega’s een universeel toepasbaar optothermisch pincetplatform, bekend als CRISPR-aangedreven optothermische nanotweezers, om bionanodeeltjes te identificeren en gebruikten ze de opstelling om in situ DNA-moleculen te identificeren, zonder nucleïnezuuramplificatie. De experimenten leverden ultralage detectievolumes op van 10 μl om polymorfismen van één nucleotide te identificeren om de genetische diversiteit te bestuderen, ziektegevoeligheid en medicijnresponsom te voldoen aan de toekomstige eisen van genomisch onderzoek en geneeskunde.
Het werkingsprincipe
Om CRONT (CRISPR-aangedreven optothermische nanotweezers) mogelijk te maken, ontwierpen de wetenschappers een microfluïdische kamer met een dunne laag goudfilm op het dekglas. Toen het team de goudfilm bestraalde met laserverlichting, genereerden ze een temperatuurveld rond de laservlek. De wetenschappers hebben de optimale omstandigheden van CRISPR-reacties gedetailleerd beschreven en de splitsing van het DNA-goud-nanofilm-conjugaat in gang gezet, met behulp van donkerveldmicroscopie.
Ze voegden een niet-ionisch polymeer toe polyethyleenglycol (PEG) in de wateroplossing als biologische oppervlakteactieve stof uitstekende biocompatibiliteit.
De aanwezigheid van meerdere nanodeeltjes en hun variërende thermoforetische mobiliteit genereerden een duidelijke concentratie opgeloste stoffen. Wanneer opgeloste stoffen met verhoogde concentraties die met lagere concentraties beïnvloedden door osmotische druk, resulteerden de uitkomsten in een interactie die bekend staat als de diffusioforetische kracht. Dit systematische onderzoek benadrukte het potentieel voor CRONT om te worden opgenomen om biomoleculaire identificatie uit te voeren.
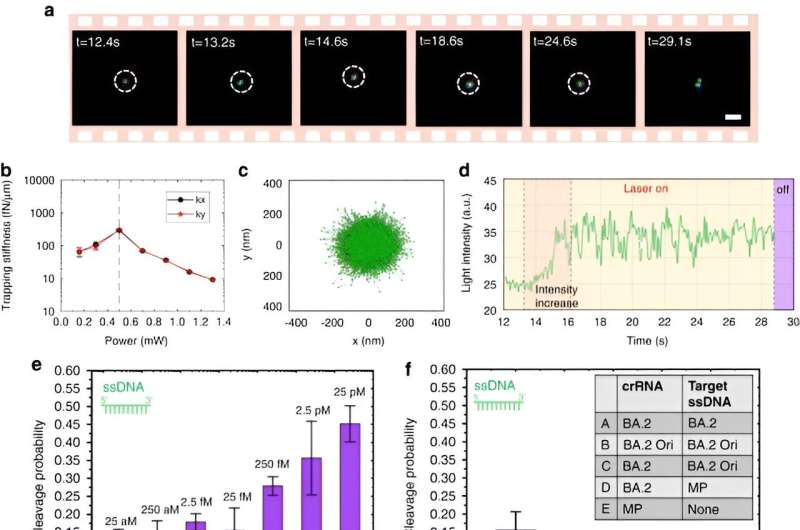
CRONT-systeem voor nucleotidedetectie en identificatie. a) Eén enkel DNA@AuNS wordt opgevangen door de CRONT in het laserverwarmingsgebied. De verwarmingslaser wordt na 28,8 seconden uitgeschakeld en daarna wordt splitsing waargenomen. b) Metingen van de trapstijfheid bij variërende laservermogens in de x/y-richting, waarbij de stippellijn de maximale stijfheid bij 0,5 mW aangeeft. c) Positieverdeling van het gevangen enkele DNA@AuNS bij 0,5 mW. d) Variatie van de lichtintensiteit van een gevangen DNA@AuNS tijdens de laseractivering. Het doel-ssDNA is afkomstig van een deel van de Monkeypox (MP)-virussequentie. Frames werden opgenomen met behulp van donkerveldmicroscopie en de schaalbalk is 2 μm. e) Splitsingswaarschijnlijkheid van het DNA@AuNS bij verschillende doel-ssDNA (MP)-concentraties. f) De waarschijnlijkheid van splitsing bij verschillende crRNA- en doel-ssDNA-combinatiegroepen (AE) voor specificiteitstests, de doel-ssDNA-concentraties zijn 250 fM. g) Splitsingswaarschijnlijkheid van het DNA@AuNS bij verschillende doel-dsDNA (MP)-concentraties. Het optische vermogen is ingesteld op 0,5 mW in (a), (c – g). h) Splitsingswaarschijnlijkheid van het DNA@AuNS onder dsDNA bij een lager optisch vermogen van 0,16 mW, de inzet geeft de temperatuurverdeling aan. Elke vastleggebeurtenis werd gedurende 2 minuten uitgevoerd en elk datapunt omvatte 10-17 vastleggebeurtenissen over een periode van 40 minuten. Elke concentratie werd driemaal getest. De PEG-massafractie bedraagt 10%. De concentratie van AuNS en Cas12a is respectievelijk 0,5 μM en 0,125 nM. Credit: Licht: Wetenschap en toepassingen, doi: 10.1038/s41377-023-01326-9
Optothermisch combineren van eiwitten en DNA’s
Om CRISPR-aangedreven optothermische nanopincetten mogelijk te maken, bestudeerden Chen en collega’s het aggregatiegedrag van eiwitten en DNA’s door gebruik te maken van fluorescentielabeling waarbij de lengte van de stijve stengel een concentratiegradiënt van polyethyleenglycol genereerde. Terwijl een hoger laservermogen de accumulatiesnelheid niet continu verhoogde als gevolg van een vergrote thermo-osmotische stroom, de accumulatie van enkelstrengs DNA was hoger dan dubbelstrengig DNA. Hoewel eiwitaccumulaties zelden worden bestudeerd in de biofysica, wordt het fluorescentie-gelabeld Cas12a-eiwitten vertoonden de neiging om lichte ringachtige ophopingen te vormen, waarbij het vergroten van het laservermogen hun accumulatiesnelheid verhoogde.
Het team voerde bovendien experimenten uit met veelgebruikte eiwitten zoals runderserumalbumine met FITC-label. In aanwezigheid van een optothermisch veld bleef deze eiwitverdeling willekeurig en niet beïnvloed door de aanwezigheid van polyethyleenglycolmoleculen.
CRISPR-aangedreven optothermische nanotweezers (CRONT) om nucleotiden te identificeren
Chen en zijn team merkten op hoe het optothermische veld geassocieerd met de CRISPR-aangedreven optothermale nanotweezers (CRONT) een geschikte temperatuur opleverde voor op CRISPR gebaseerde biodetectie, met het vermogen om bionanodeeltjes te verrijken om DNA te detecteren bij ultralage concentraties, in plaats van Brownse beweging alleen dat wordt geregeld door de detectie van diffusie.
De wetenschappers hebben onder meer het CRISPR-12a-schema onderzocht enkelstrengs omgevings-DNA. Het CRONT-systeem identificeerde met succes DNA’s op het niveau van één molecuul enkelvoudige nucleotide polymorfologieën met een hoge sensitiviteit en specificiteit.
Vooruitzichten
Op deze manier integreerden Jiajie Chen en collega’s difusioforese en thermo-osmotische stromingen in de grenslaag van een optothermische responsieve film om een nieuwe methode te tonen om CRISPR-aangedreven optothermische nanopincetten op nanoschaal te reguleren.
Deze methode maakte de onmiddellijke implementatie van op CRISPR gebaseerde biosensoren met een ultralaag detectievolume mogelijk.
Optische pincetten zijn voorzien van DNA-identificatie via op CRISPR gebaseerde biosensorsystemen als een manier voor verrijking van biomoleculen om het CRISPR-complex te splitsen. Dergelijke CRISPR-aangedreven optothermische nanopincetten of CRONT-systemen houden een enorme belofte in om het begrip van complexe biologische processen te bevorderen als een veelzijdige detectiesonde in biomedisch onderzoek, medicijnontdekking en ziektediagnostiek.
Meer informatie:
Jiajie Chen et al, CRISPR-aangedreven optothermische nanopincet: diverse manipulatie van bio-nanodeeltjes en identificatie van enkele nucleotiden, Licht: wetenschap en toepassingen (2023). DOI: 10.1038/s41377-023-01326-9
Tijdschriftinformatie:
Licht: wetenschap en toepassingen