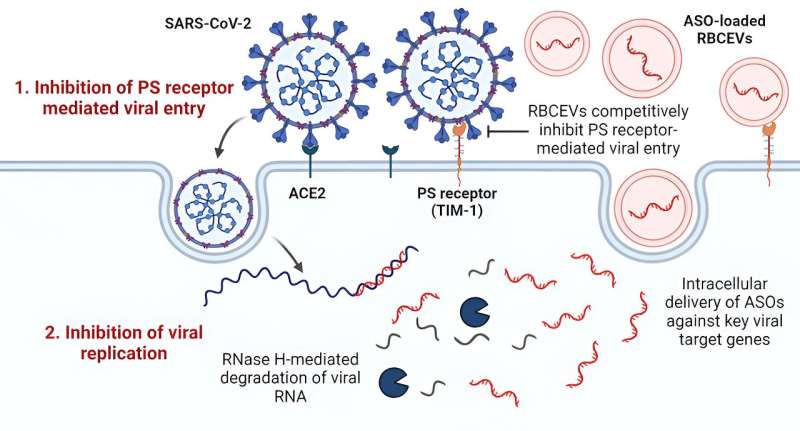
Mechanisme van door extracellulaire blaasjes (EV) gemedieerde SARS-CoV-2-remming. Credit:ACS Nano (2023). DOI: 10.1021/acsnano.3c06803
De COVID-19-pandemie heeft aangetoond hoe belangrijk het is voorbereid te zijn met medicamenteuze interventies om virusuitbraken in te dammen die anders verwoestende gevolgen kunnen hebben. Bij de voorbereiding op de volgende pandemie – of Ziekte X – is er dringend behoefte aan veelzijdige platformtechnologieën die op korte termijn opnieuw kunnen worden ingezet om infectieuze uitbraken te bestrijden.
Een team van onderzoekers, onder leiding van assistent-professor Minh Le van het Institute for Digital Medicine (WisDM) en de afdeling Farmacologie van de Yong Loo Lin School of Medicine, National University of Singapore (NUS Medicine), ontdekte dat nanodeeltjes die vrijkomen door cellen, ‘extracellulaire blaasjes’ (EV’s) genoemd, kunnen de virale infectiviteit van SARS-CoV-2 – de wildtype en varianten ervan – en mogelijk andere infectieziekten beteugelen.
Asst Prof Le zei: “Ons onderzoek heeft aangetoond dat deze van cellen afkomstige nanodeeltjes effectieve dragers zijn van medicijnen die zich precies op virale genen richten. Deze EV’s zijn daarom een efficiënt hulpmiddel voor therapeutische interventie bij patiënten die besmet zijn met COVID-19 of andere infectieuze ziekten. ziekten.”
De studie, uitgevoerd in samenwerking met de Biosafety Level 3 (BSL3) Core Facility van NUS Medicine, het Cancer Science Institute of Singapore van de National University of Singapore, en de School of Physical and Mathematical Sciences van de Nanyang Technological University (NTU), toonde een krachtige remming aan van COVID-19-infectie in laboratoriummodellen met behulp van een combinatie van op EV gebaseerde remming en antisense RNA-therapie gemedieerd door antisense oligonucleotiden (ASO’s).
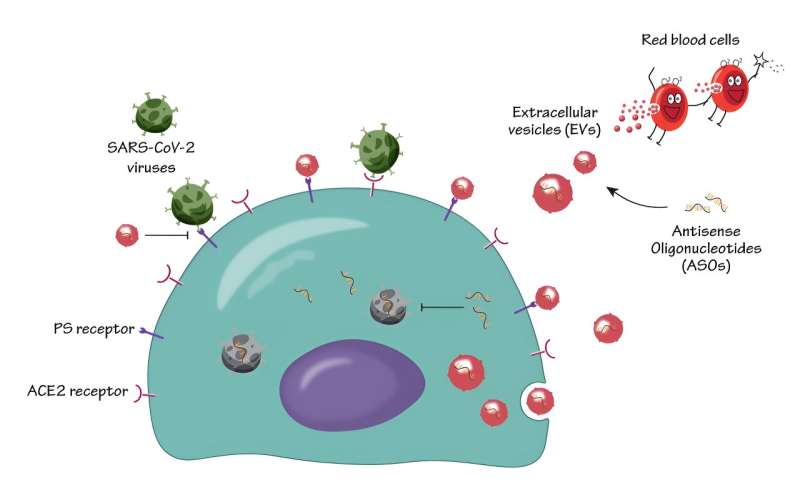
Remming van SARS-CoV-2-virusinfectie door extracellulaire blaasjes van rode bloedcellen (RBCEV’s). Krediet: Trinh Tran
Een veelzijdig hulpmiddel dat op elk gen van belang kan worden toegepast. ASO’s kunnen complementaire regio’s van doel-RNA-moleculen herkennen en daaraan binden en hun remming en afbraak induceren.
In het onderzoek, gepubliceerd in ACS Nanogebruikten de auteurs van menselijke rode bloedcellen afkomstige EV’s om ASO’s af te leveren op belangrijke plaatsen die besmet waren met SARS-CoV-2, wat resulteerde in een efficiënte onderdrukking van SARS-CoV-2-infectie en -replicatie.
De onderzoekers ontdekten ook dat EV’s verschillende antivirale eigenschappen vertoonden, die in staat zijn om door fosfatidylserine (PS)-receptor gemedieerde routes van virale infecties te remmen – een belangrijke route die door veel virussen wordt gebruikt om virale infecties te vergemakkelijken. Deze virusremmende mechanismen waren toepasbaar op meerdere varianten van SARS-CoV-2, waaronder de delta- en omicron-stammen, waardoor hun brede effectiviteit tegen SARS-CoV-2-infectie werd gegarandeerd.
De resultaten van het onderzoek wijzen op antisense-RNA-therapie met ASO’s als een potentieel effectieve aanpak die zou kunnen dienen om toekomstige virale uitbraken te bestrijden. Het platform dat werd ontwikkeld om ASO’s via EV’s af te leveren om zich te richten op de virale SARS-CoV-2-genen, kan gemakkelijk worden toegepast om andere virale infecties te behandelen door de ASO-sequenties te vervangen door de sequenties die complementair zijn aan de virale doelgenen.
Asst Prof Le en haar afgestudeerde studenten Migara Jay en Gao Chang, de eerste auteurs van de studie, ontwikkelen momenteel krachtigere combinaties van ASO’s met behulp van voorspellingsmodellen voor kunstmatige intelligentie om verbeterde virale remming te bereiken. Deze gezamenlijke inspanning omvat een partnerschap met de onderzoeksteams van universitair hoofddocent Edward Chow van WisDM, NUS Medicine en de BSL3 Core Facility van NUS Medicine.
Universitair hoofddocent Justin Chu, directeur van de BSL3 Core Facility bij NUS Medicine en co-auteur van de studie, voegde hieraan toe: “Deze opmerkelijke extracellulaire, op blaasjes gebaseerde platformtechnologie in combinatie met antivirale therapie is zeer veelbelovend om een breed scala aan virussen te bestrijden. en zelfs Ziekte X.”
Dit laatste is een algemene beschrijving van opkomende en onbekende infectiedreigingen, zoals nieuwe coronavirussen. De term werd gebruikt om de ontwikkeling van platformtechnologieën te waarschuwen en aan te moedigen, waaronder vaccins, medicijntherapieën en diagnostische tests, die snel konden worden aangepast en vervolgens konden worden ingezet tegen toekomstige uitbraken van epidemieën en pandemieën. Assoc Prof Chu is ook lid van het Infectious Diseases Translational Research Program bij NUS Medicine.
Professor Dean Ho, voorzitter van Provost en directeur van WisDM bij NUS Medicine, zei: “Dit werk brengt het schaalbare en goed getolereerde extracellulaire, op blaasjes gebaseerde medicijnafgifteplatform een belangrijke stap dichter bij klinische validatiestudies.”
Meer informatie:
Migara K. Jayasinghe et al., Van rode bloedcellen afkomstige extracellulaire blaasjes vertonen endogene antivirale effecten en verbeteren de werkzaamheid van antivirale oligonucleotidetherapie, ACS Nano (2023). DOI: 10.1021/acsnano.3c06803
Tijdschriftinformatie:
ACS Nano
Aangeboden door de Nationale Universiteit van Singapore