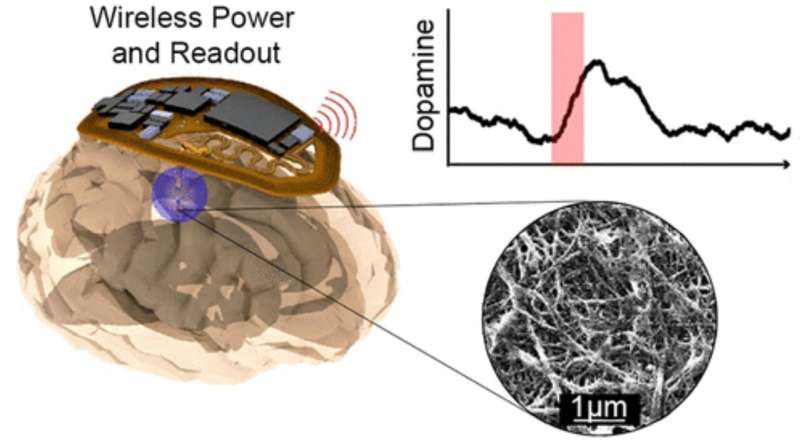
Grafisch abstract. Credit: ACS Nano (2022). DOI: 10.1021/acsnano.2c09475
Wetenschappers hebben een draadloos, batterijloos implantaat ontwikkeld dat in staat is om dopaminesignalen in de hersenen in real-time te volgen in kleine diermodellen, een vooruitgang die zou kunnen helpen bij het begrijpen van de rol die neurochemicaliën spelen bij neurologische aandoeningen.
Het apparaat, beschreven in een studie gepubliceerd in ACS Nano, activeert of remt specifieke neuronen in de hersenen met behulp van licht, een techniek die bekend staat als optogenetische stimulatie. Het registreert ook de dopamine-activiteit bij proefpersonen die zich vrij gedragen zonder de noodzaak van omvangrijke of belemmerende detectieapparatuur, aldus John Rogers, Ph.D., de Louis Simpson en Kimberly Querrey Professor of Materials Science and Engineering, Biomedical Engineering en Neurological Surgery, en een co – auteur van de studie.
“Met dit apparaat kunnen neurowetenschappers de hersenactiviteit in realtime en op een programmeerbare manier volgen en moduleren, bij muizen – een zeer belangrijke klasse van diermodellen voor neurowetenschappelijke studies,” zei Rogers.
“De miniatuurgrootte van het apparaat, de extreem lichte constructie en de draadloze, batterijloze werking maken gedragsstudies mogelijk die anders onmogelijk zouden zijn. We kunnen zien hoe de hersenen werken terwijl een dier beweegt en zich bezighoudt met natuurlijke omgevingen in een onbelemmerde manier, in geïsoleerde individuen of in sociaal interagerende groepen.”
Om het apparaat te maken, ontwierpen onderzoekers eerst een geminiaturiseerde dopaminesensor met behulp van koolstofvezelcomposietelektroden om de hoogst mogelijke gevoeligheid te bieden. Vervolgens implementeerden ze draadloze, batterijloze elektronische circuits die werden gevoed via externe transmissieantennes en vervaardigden ze het apparaat met behulp van laserpatronen en dunne filmafzetting om een klein, flexibel implantaat te creëren.
Volgens de auteurs van het onderzoek is het apparaat 50 keer lichter en 10 keer kleiner dan het meest geavanceerde alternatief.
In de studie was het apparaat in staat om hersengebieden te stimuleren en dopamine-activiteit vast te leggen als reactie op blootstelling aan opioïden en naloxon in muismodellen.
De technologie zal nuttig zijn bij het bestuderen van hoe neurochemicaliën gedrag, verslaving en de ontwikkeling van neurologische ziekten beïnvloeden, zei Philipp Gutruf, Ph.D., assistent-professor Biomedical Engineering aan de Universiteit van Arizona en senior auteur van de studie.
“Neurochemische samenstelling in de hersenen is een gebied dat, vanwege de huidige beperking van onderzoeksinstrumenten, niet zo goed wordt begrepen als elektrische activiteit”, zegt Gutruf, een voormalig postdoctoraal onderzoeker in het Rogers-laboratorium. “Er is echter aangegeven dat neurochemische samenstelling erg belangrijk is bij de behandeling en detectie van neurodegeneratieve ziekten zoals de ziekte van Alzheimer en Parkinson. Vooruitgang die door ons werk wordt geïntroduceerd, zal de neurowetenschappelijke gemeenschap helpen fundamentele mechanismen te begrijpen en nieuwe therapiekandidaten te valideren.”
In de toekomst hopen de auteurs van het onderzoek het apparaat te verfijnen en commercieel beschikbaar te maken, zei Rogers.
“We willen de chemische detectiemogelijkheden uitbreiden naar andere neurotransmitters naast dopamine en ervoor zorgen dat het tegelijkertijd met meerdere hersengebieden kan communiceren”, zegt Rogers, die ook lid is van het Robert H. Lurie Comprehensive Cancer Center van Northwestern University. “Bovendien willen we deze technologie op een goedkope manier beschikbaar stellen aan de bredere gemeenschap van neurowetenschappers om hun eigen onderzoeksinspanningen te vergemakkelijken.”
Meer informatie:
Tucker Stuart et al., Draadloze, batterijloze implantaten voor elektrochemische catecholaminedetectie en optogenetische stimulatie, ACS Nano (2022). DOI: 10.1021/acsnano.2c09475
Tijdschrift informatie:
ACS Nano
Aangeboden door Northwestern University