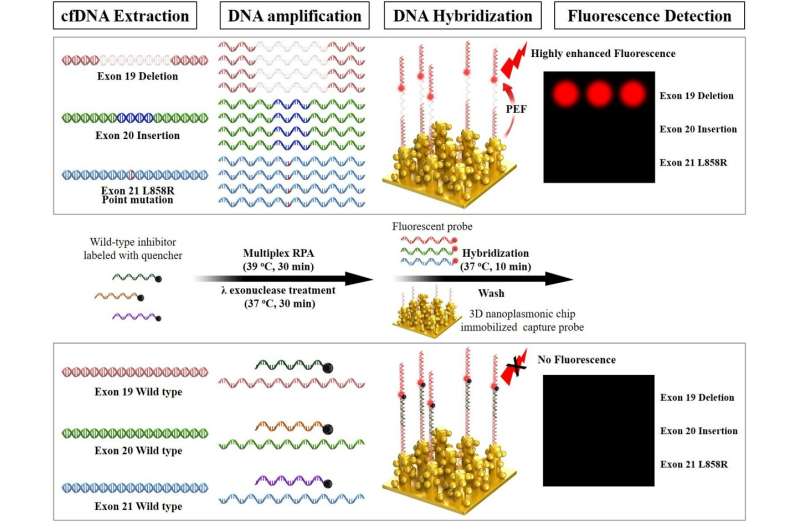
Assayproces van de EGFR-mutatie multi-analysechip. Credit: Korea Institute of Materials Science (KIMS)
Dr. Min-young Lee en Dr. Sung-gyu Park van de Advanced Bio and Healthcare Materials Research Division bij KIMS hebben een technologie ontwikkeld die kankermutante genen in bloed kan detecteren met ’s werelds hoogste gevoeligheid van 0,000000001% op basis van plasmonische nanomaterialen voor optische signaalversterking. Het team testte bloedmonsters van longkankerpatiënten (stadia 1-4) en gezonde individuen op EGFR-mutaties en bereikte een diagnostische nauwkeurigheid van 96%.
Het werk is gepubliceerd in het dagboek Kleine wetenschap.
Eerder gebruikte genetische analysetechnologieën hadden een lage analytische gevoeligheid om gemuteerde genen te detecteren in vergelijking met normale genen, waardoor het moeilijk was om kankerpatiënten in een vroeg stadium nauwkeurig te diagnosticeren. Bovendien was het moeilijk om een snelle behandelstrategie op te stellen en deze toe te passen op screeningtests vanwege de hoge kosten en de lange tijd die nodig was voor analyse en de noodzaak van speciale apparatuur.
Om deze uitdagingen te overwinnen, ontwikkelde het onderzoeksteam een goedkope analysetechnologie die verschillende kankermutaties binnen het doelgengebied binnen één uur kan analyseren met een ultrahoge gevoeligheid van 0,000000001%. Deze technologie heeft het hoogste gevoeligheidsniveau ter wereld, dat 100.000 keer beter is dan het hoogste niveau van 0,0001% onder gerapporteerde technologieën, en hierdoor werd de mogelijkheid van vroege diagnose bevestigd met behulp van het bloed van longkankerpatiënten.
Deze technologie combineert nanomateriaaltechnologie die het fluorescentiesignaal aanzienlijk verbetert, en primer/probe-ontwerp dat het fluorescentiesignaal van normale genen onderdrukt en alleen het fluorescentiesignaal van kankermutante genen versterkt. Dit komt omdat de nauwkeurige detectie van zelfs zeer kleine hoeveelheden kankermutante genen niet alleen sterke fluorescentiesignaalexpressietechnologie vereist, maar ook nauwkeurige discriminatie van fijne fluorescentiesignalen.
Het team fabriceerde een biochip in de vorm van een microarray die in staat is om gelijktijdig drie gemuteerde genen van EGFR (deletie, insertie en puntmutaties) te detecteren op een plasmonisch substraat gemaakt van driedimensionale, high-density goud nanostructuren. Na evaluatie van de klinische prestaties van 43 binnenlandse longkankerpatiënten (stadia 1 tot 4) en 40 normale groepen, werd een klinische gevoeligheid van 93% voor longkankerpatiënten en een klinische specificiteit van 100% voor de normale groep bevestigd.
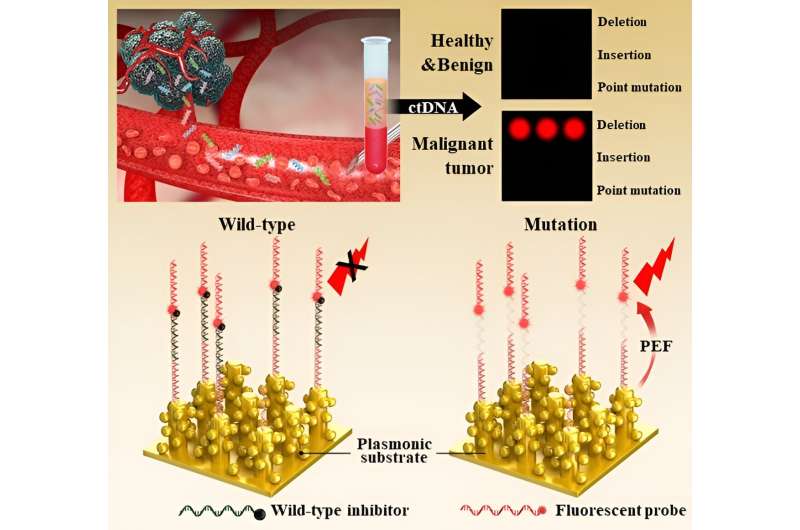
Representatief diagram van 3D nanoplasmonics-gebaseerde technologie voor het detecteren van mutante genen in bloed. Credit: Korea Institute of Materials Science (KIMS)
Deze technologie kan een belangrijke rol spelen bij niet alleen vroege diagnose en detectie van terugkeer van kanker, maar ook bij het monitoren van de effectiviteit van de behandeling en het opstellen van gepersonaliseerde behandelplannen. Daarnaast is vloeibare biopsie met behulp van bloed mogelijk als alternatief voor chirurgische weefselbiopsie, wat de belasting voor patiënten vermindert en het onderzoeksproces vereenvoudigt. Het kan ook dienen als een reguliere screeningtest, wat uiteindelijk de kwaliteit van kankermanagement en -behandeling verbetert.
Senior onderzoeker Min-young Lee zei: “Omdat het in staat is om verschillende kankermutaties uitgebreid te detecteren met ’s werelds hoogste niveau van ultrahoge gevoeligheid, kan het een toonaangevende speler worden in de markt voor vroege kankerdiagnose en behandeling/terugkeermonitoring. We verwachten dat dit de overlevingskans en de kwaliteit van leven van kankerpatiënten aanzienlijk zal verbeteren.”
Meer informatie:
Ji Young Lee et al, Zeer gevoelige 3D-nanoplasmonic-gebaseerde epidermale groeifactorreceptormutatiemultiplex-assaychip voor vloeibare biopsie, Kleine wetenschap (2024). DOI-bestand: 10.1002/smsc.202400101
Aangeboden door de National Research Council of Science and Technology