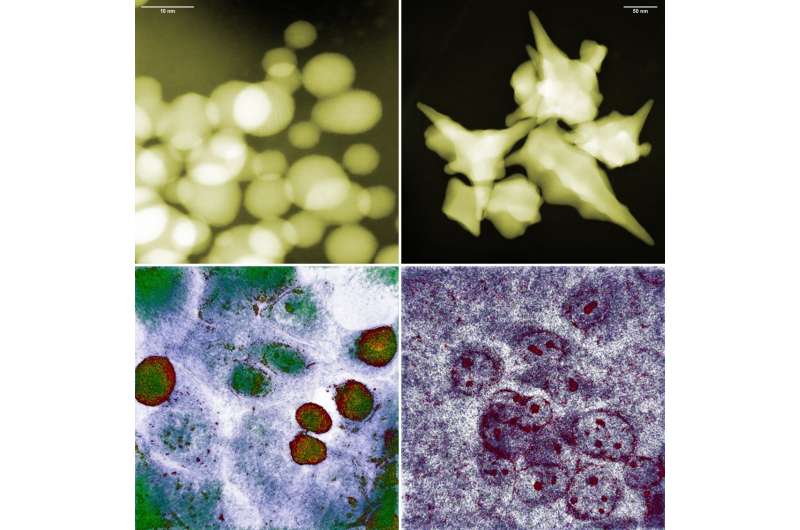
Bolvormige en stervormige gouden nanodeeltjes (boven) en darmkankercellen na ca. vijf uur blootstelling eraan (respectievelijk onderaan). De foto linksonder bewijst dat de kankercellen ondanks het kleine formaat van de bolvormige nanodeeltjes overleefden. Valse kleuren. Krediet: IFJ PAN
Gouddeeltjes ter grootte van miljardsten van een meter zijn dodelijk voor kankercellen. Dit feit is al lang bekend, evenals een eenvoudige correlatie: hoe kleiner de nanodeeltjes die worden gebruikt om de kankercellen te bestrijden, hoe sneller ze afsterven. Er komt echter een interessanter en complexer beeld van deze interacties naar voren uit het laatste onderzoek, uitgevoerd aan het Instituut voor Kernfysica van de Poolse Academie van Wetenschappen, met behulp van een nieuwe microscopische techniek.
Kleinere moorden zijn sneller – dit is wat eerder werd gedacht over gouden nanodeeltjes die worden gebruikt om kankercellen te bestrijden. Wetenschappers dachten dat kleine nanodeeltjes het eenvoudigweg gemakkelijker zouden vinden om het inwendige van een kankercel binnen te dringen, waar hun aanwezigheid zou leiden tot metabolische stoornissen en uiteindelijk celdood.
De werkelijkheid blijkt echter complexer te zijn, zoals blijkt uit onderzoek uitgevoerd door wetenschappers van het Instituut voor Kernfysica van de Poolse Academie van Wetenschappen (IFJ PAN) in Krakau, ondersteund door theoretische analyses uitgevoerd aan de Universiteit van Rzeszow (UR) en de Technische Universiteit van Rzeszow.
“Ons instituut beheert een geavanceerd medisch en acceleratorcentrum voor protonenradiotherapie. Dus toen er een paar jaar geleden berichten verschenen dat gouden nanodeeltjes goede radiosensitizers zouden kunnen zijn en de effectiviteit van dit soort therapie zouden kunnen verbeteren, zijn we begonnen ze te synthetiseren onszelf en testen hun interactie met kankercellen. We kwamen er al snel achter dat de toxiciteit van nanodeeltjes niet altijd was zoals verwacht”, zegt dr. Joanna Depciuch-Czarny (IFJ PAN), initiatiefnemer van het onderzoek en eerste auteur van een artikel waarin de resultaten worden besproken. , gepubliceerd in het dagboek Klein.
Nanodeeltjes kunnen worden geproduceerd met behulp van verschillende methoden, waardoor deeltjes van verschillende groottes en vormen ontstaan. Kort nadat ze hun eigen experimenten met gouden nanodeeltjes begonnen, merkten de natuurkundigen van het IFJ PAN op dat biologie niet de populaire regel volgt dat hun toxiciteit groter is naarmate ze kleiner zijn.
Sferische nanodeeltjes van 10 nanometer groot, geproduceerd in Krakau, bleken praktisch ongevaarlijk voor de bestudeerde glioomcellijn. Er werd echter een hoge mortaliteit waargenomen in cellen die werden blootgesteld aan nanodeeltjes van wel 200 nanometer groot, maar met een stervormige structuur.
Opheldering van de genoemde tegenstrijdigheid werd mogelijk dankzij het gebruik van de eerste holotomografische microscoop in Polen, bij IFJ PAN.
Een typische CT-scanner scant het menselijk lichaam met behulp van röntgenstralen en reconstrueert de ruimtelijke interne structuur sectie voor sectie. In de biologie is onlangs een soortgelijke functie uitgevoerd door de holotomografische microscoop. Hier worden de cellen ook belaagd door een stralingsbundel, maar dan geen hoogenergetische straling, maar elektromagnetische straling. De energie ervan is zo gekozen dat de fotonen het celmetabolisme niet verstoren.
Het resultaat van de scan is een set holografische dwarsdoorsneden met informatie over de verdeling van veranderingen in de brekingsindex. Omdat licht anders breekt op het cytoplasma en anders op het celmembraan of de celkern, is het mogelijk om een driedimensionaal beeld te reconstrueren van zowel de cel zelf als het inwendige ervan.
“In tegenstelling tot andere microscopietechnieken met hoge resolutie vereist holotomografie geen voorbereiding van monsters of de introductie van vreemde stoffen in de cellen. De interacties van gouden nanodeeltjes met kankercellen konden daarom rechtstreeks in de incubator worden waargenomen, waar deze werden gekweekt , in een ongestoorde omgeving – bovendien met nanometrische resolutie – van alle kanten tegelijk en praktisch in realtime”, somt Dr. Depciuch-Czarny op.
Dankzij de unieke kenmerken van holotomografie konden natuurkundigen de oorzaken van het onverwachte gedrag van kankercellen in de aanwezigheid van gouden nanodeeltjes vaststellen. Er werd een reeks experimenten uitgevoerd met drie cellijnen: twee gliomen en één colon. Er werd onder meer waargenomen dat hoewel de kleine, bolvormige nanodeeltjes gemakkelijk de kankercellen binnendrongen, de cellen zich regenereerden en zelfs weer begonnen te delen, ondanks de aanvankelijke stress.
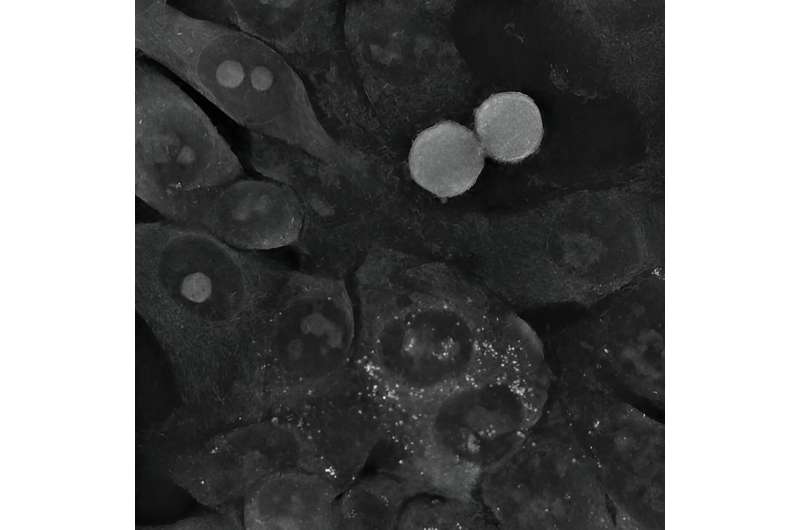
Colonkankercellen veranderden na interactie met kleine bolvormige goudnanodeeltjes niet van morfologie en konden zich nog steeds delen. Credit: IFJ PAN
In het geval van darmkankercellen werden de gouden nanodeeltjes er snel uit geduwd. Voor de grote stervormige nanodeeltjes was de situatie anders. Hun scherpe punten perforeerden de celmembranen, wat hoogstwaarschijnlijk resulteerde in toenemende oxidatieve stress in de cellen. Toen deze cellen het herstel van de toenemende schade niet langer aankonden, werd het mechanisme van apoptose, oftewel geprogrammeerde dood, in werking gesteld.
“We hebben de gegevens van de experimenten in Krakau gebruikt om een theoretisch model op te bouwen van het proces van de afzetting van nanodeeltjes in de onderzochte cellen. Het eindresultaat is een differentiaalvergelijking waarin op de juiste manier verwerkte parameters kunnen worden vervangen – voorlopig beschrijft het alleen de vorm en de grootte van nanodeeltjes – om snel te bepalen hoe de opname van de geanalyseerde deeltjes door kankercellen over een bepaalde periode zal verlopen”, zegt Dr. Pawel Jakubczyk, professor aan de UR en co-auteur van het model.
Hij benadrukt: “Elke wetenschapper kan ons model al in de ontwerpfase van zijn eigen onderzoek gebruiken om direct het aantal varianten van nanodeeltjes te beperken dat experimentele verificatie vereist.”
Het vermogen om het aantal potentiële experimenten dat moet worden uitgevoerd eenvoudig te verminderen, betekent een vermindering van de kosten die gepaard gaan met de aankoop van cellijnen en reagentia, evenals een duidelijke vermindering van de onderzoekstijd (het duurt doorgaans ongeveer twee weken om alleen al een commercieel verkrijgbare cellijn te kweken). Bovendien kan het model worden gebruikt om beter gerichte therapieën te ontwerpen dan voorheen – therapieën waarbij de nanodeeltjes bijzonder goed worden geabsorbeerd door geselecteerde kankercellen, terwijl de toxiciteit voor gezonde cellen in de andere organen van de patiënt relatief laag of zelfs nul blijft.
De Krakau-Rzeszow-groep van wetenschappers bereidt zich al voor om hun onderzoek voort te zetten. Nieuwe experimenten zouden het binnenkort mogelijk moeten maken om het model van de interactie van nanodeeltjes met kankercellen uit te breiden met verdere parameters, zoals de chemische samenstelling van de deeltjes of verdere tumortypen. Latere plannen omvatten ook het aanvullen van het model met wiskundige elementen om de werkzaamheid van foto- of protontherapie voor geïndiceerde combinaties van nanodeeltjes en tumoren te optimaliseren.
Meer informatie:
Joanna Depciuch et al, Modellering van de absorptiedynamiek van verschillend gevormde goudglioblastoom- en coloncellen op basis van de brekingsindexverdeling in holotomografische beeldvorming, Klein (2024). DOI: 10.1002/smll.202400778
Informatie over het tijdschrift:
Klein
Geleverd door de Poolse Academie van Wetenschappen