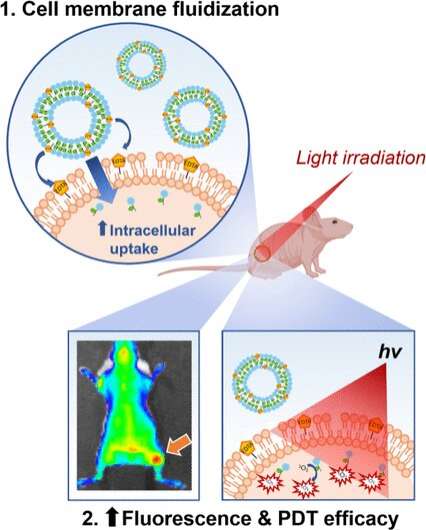
Credit: Angewandte Chemie International Edition (2023). DOI: 10.1002/anie.202218218
Om kankermedicijnen aan tumorcellen te leveren, moeten de celmembranen worden doorbroken. Een team van onderzoekers heeft een eenvoudige manier ontdekt om dit te bereiken met behulp van lipide nanodeeltjes die het reagens EDTA (ethyleendiaminetetra-azijnzuur) bevatten. Zoals het team rapporteert in het tijdschrift Angewandte Chemieis een ongebruikelijk werkingsmechanisme van EDTA verantwoordelijk voor dit nuttige effect.
Een van de grootste uitdagingen bij kankertherapie is de gerichte toediening van medicijnen, vervat in nanodeeltjes, aan tumorcellen, waar ze de cellen vervolgens kunnen doden. Helaas zijn celmembranen zeer selectief in termen van wat ze doorlaten. Receptoren op het membraanoppervlak fungeren meestal als poortwachters, maar het is lastig om de precieze moleculaire sleutel te bedenken om ze te ontgrendelen.
Liposomen bieden één alternatief: deze lipidebolletjes op nanoschaal versmelten simpelweg met het celmembraan en transporteren daarbij hun therapeutische lading naar de cel. Er wordt echter nog steeds gezocht naar een efficiëntere intracellulaire opname om de werkzaamheid van geneesmiddelen te vergroten.
Gang Zheng en collega’s van het Princess Margaret Cancer Centre en de Universiteit van Toronto, Canada, hebben EDTA nader bekeken als een nieuwe manier om toegang te krijgen tot kankercellen. EDTA kan metaalionen cheleren, met andere woorden ze veilig binden en uit hun omgeving verwijderen. In de biogeneeskunde wordt EDTA gebruikt om vergiftiging door zware metalen te behandelen en wordt het gebruikt als contrastmiddel voor bioimaging.
Zheng en het team veronderstelden dat het chelerende effect ook nuttig zou kunnen zijn als celopener. Zoals Zheng uitlegt: “Het is bekend dat een hoge concentratie EDTA bacteriële membranen permeabel maakt door metalen (bijv. concentratie die niet giftig is voor menselijke cellen.”
Het team nam daarom een EDTA-lipideverbinding op in met medicijnen beladen liposomen, om ze in tumorcellen af te leveren. De experimentele resultaten overtroffen zelfs hun verwachtingen en toonden een drastisch verbeterde internalisatie in zowel cellijnen als in een muismodel. Bij met tumor geïnfecteerde muizen veroorzaakte het medicijn – porfyrines gebruikt voor fotodynamische therapie – dat de tumor achteruitging en verbeterde de overlevingspercentages van de muizen aanzienlijk.
Tot grote verrassing van het team had het chelaateffect echter niets te maken met de verbeterde internalisatie. “Dit proces is volledig onafhankelijk van zijn metaalchelatie-eigenschappen”, zegt Zheng over de bevindingen van het team. In plaats daarvan ontdekte de groep dat EDTA werkte als een reinigingsmiddel om de kenmerken van het celmembraan te veranderen, waardoor het vloeibaarder en flexibeler werd om de opname van nanodeeltjes te bevorderen.
De groep is nu van plan dit nieuw ontdekte mechanisme toe te passen op een algemene op EDTA-lipiden gebaseerde strategie voor cellen om liposomale nanodeeltjes te absorberen voor verbeterde therapie.
Meer informatie:
Tiffany Ho et al, Nieuwe strategie om de intracellulaire opname van lipide nanodeeltjes voor fotodynamische therapie te stimuleren, Angewandte Chemie International Edition (2023). DOI: 10.1002/anie.202218218
Tijdschrift informatie:
Angewandte Chemie International Edition
,
Angewandte Chemie
Aangeboden door Wiley