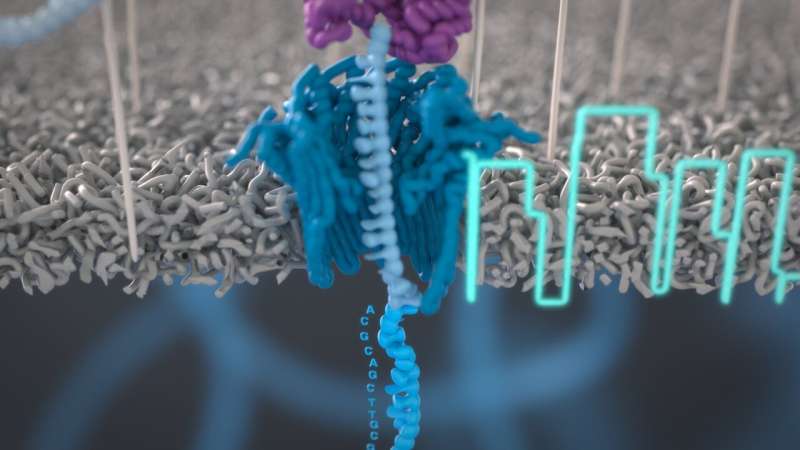
Illustratie van een nanoporie die een DNA-sequentie afleest en deze omzet in een elektrisch signaal. Krediet: Oxford Nanopore
Met de mogelijkheid om tientallen biomarkers tegelijk in kaart te brengen, zou een nieuwe methode het testen op aandoeningen als hartziekten en kanker kunnen transformeren.
Momenteel worden veel ziekten gediagnosticeerd op basis van bloedtesten waarbij wordt gezocht naar één biomarker (zoals een eiwit of een ander klein molecuul) of hoogstens naar een paar biomarkers van hetzelfde type.
De nieuwe methode, ontwikkeld door wetenschappers van het Imperial College London in een onderzoekssamenwerking met Oxford Nanopore Technologies (Oxford Nanopore), kan tientallen biomarkers van verschillende typen tegelijkertijd analyseren. Hierdoor zouden artsen mogelijk meer informatie kunnen verzamelen over de ziekte van een patiënt.
De huidige tests voor hartfalen zoeken bijvoorbeeld naar een aantal veel voorkomende eiwitten om te bepalen of de aandoening aanwezig is. De nieuwe methode kon bovendien 40 verschillende soorten miRNA-moleculen detecteren, die het potentieel hebben om te worden gebruikt als een nieuwe klasse biomarkers. Het kan tegelijkertijd eiwitten, kleine moleculen zoals neurotransmitters en miRNA uit hetzelfde klinische monster onderzoeken, waardoor uitgebreide gegevens worden verkregen voor een nauwkeurigere diagnose.
De resultaten van het op deze manier toepassen van de nieuwe test met het bloed van gezonde deelnemers, voor een proof-of-concept onderzoek, zijn gepubliceerd in Natuur Nanotechnologie.
Co-eerste auteur Caroline Koch, van de afdeling Scheikunde van Imperial, zei: “Er zijn veel verschillende manieren waarop je tot hartfalen kunt komen, maar onze test zal hopelijk een goedkope en snelle manier bieden om dit uit te zoeken en je te helpen bij het begeleiden van hartfalen.” “Behandelingsopties. Dit soort resultaten zijn mogelijk met minder dan een milliliter bloed. Het is ook een zeer aanpasbare methode, zodat deze door het veranderen van de doelbiomarkers kan worden gebruikt om de kenmerken van ziekten, waaronder kanker en neurodegeneratieve aandoeningen, te detecteren.”
Co-eerste auteur Ben Reilly-O’Donnell, van het National Heart and Lung Institute in Imperial, voegde hieraan toe: “Het vermogen om verschillende soorten moleculen tegelijkertijd in hetzelfde monster te monitoren, biedt een duidelijk voordeel ten opzichte van traditionele analysemethoden. .”

Het MinION-apparaat. Krediet: Oxford Nanopore
DNA-barcodering
De test werkt door het bloedmonster te mengen met DNA-‘barcodes’. Dit zijn kleine tags gemaakt van korte DNA-sequenties, die elk coderen voor een unieke probe die is ontworpen om zich aan een andere biomarker te hechten. Zodra het monster en de streepjescodes zijn gemengd, wordt de resulterende oplossing geïnjecteerd in een goedkoop handapparaat dat eerder is ontwikkeld door Oxford Nanopore. MinION.
Het Oxford Nanopore-apparaat bevat een doorstroomcel met een reeks nanoporiën (zeer kleine gaatjes) die in staat zijn de elektrische handtekening te lezen van elke DNA-barcode die erdoorheen gaat. Het complexe elektrische signaal dat het apparaat produceert, wordt geïnterpreteerd door een machinaal leeralgoritme om het type en de concentratie van elke biomarker in het monster te identificeren.
De DNA-barcodes die voor elke test worden gebruikt, kunnen op bestelling worden gemaakt, specifiek voor de biomarkers die moeten worden geanalyseerd om de ziekte waarop wordt getest te karakteriseren. Het gebruik van DNA-barcodes maakt ook de noodzaak van complexe en tijdrovende monstervoorbereiding overbodig, wat ook tot monstervertekening kan leiden.
Hoofdonderzoeker Professor Joshua Edel, van de afdeling Scheikunde van Imperial, zei: “Door samen te werken met Oxford Nanopore Technologies zijn we erin geslaagd hun bestaande platform te gebruiken en te innoveren hoe het kan worden gebruikt, met de toevoeging van DNA-barcodes en machinaal leren om begrijp de resultaten.”
Co-hoofdonderzoeker Dr. Alex Ivanov, ook van de afdeling Scheikunde van Imperial, voegde hieraan toe: “In principe zijn we dicht bij het mogelijk maken van een technologie die geschikt is voor klinieken, waar we op de lange termijn hopen dat deze een rijkdom kan opleveren. van geïndividualiseerde informatie voor patiënten met een reeks aandoeningen.”
Toekomstige richtingen
Na te hebben aangetoond dat deze methode met succes 40 miRNA-moleculen in het bloed van gezonde patiënten kan meten, werkt het team nu met klinische monsters van patiënten met hartfalen om de resultaten te valideren. Regelmatige tests als deze kunnen artsen ook helpen bij het vaststellen van de uitgangswaarden van hun individuele patiënten voor gewone bloedbiomarkers.
De methode kan op twee manieren nuttig zijn om de diagnose te versnellen: naast het meten van meer biomarkers tegelijk, kan het ook helpen bij het vinden van nieuwe biomarkers. Hoewel momenteel slechts een handvol biomarkers gevalideerd is voor het diagnosticeren van hartziekten, zou het team, door gelijktijdig 40 miRNA-types te meten die van belang zijn, ook kunnen zien welke hiervan relevant zijn en gevalideerd kunnen worden met meer testen.
Meer informatie:
Nanopore-sequencing van sondes met DNA-barcode voor sterk gemultiplexte detectie van microRNA, eiwitten en kleine biomarkers, Natuur Nanotechnologie (2023). DOI: 10.1038/s41565-023-01479-z. www.nature.com/articles/s41565-023-01479-z
Tijdschriftinformatie:
Natuur Nanotechnologie
Geleverd door Imperial College Londen