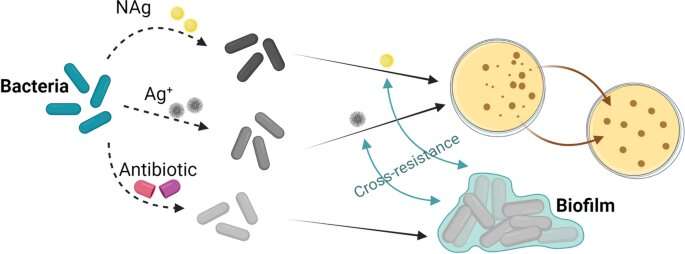
Grafisch abstract. Krediet: DOI: 10.1186/s12951-021-01027-8
Nieuw onderzoek van de University of Technology Sydney (UTS) heeft aangetoond dat ziekteverwekkers die biofilms vormen kunnen evolueren om behandeling met nanozilver te overleven. De studie is de eerste die aantoont dat een langdurige behandeling met nanozilver het risico op terugkerende infecties kan verhogen.
Het onderzoek is gepubliceerd in de Tijdschrift voor nanobiotechnologie.
Nanozilver is een krachtig antimicrobieel middel dat momenteel wordt gebruikt in medische hulpmiddelen zoals interne katheters en wondverbanden, met name voor brandwonden, om infecties te bestrijden of te voorkomen. Het is ook een van de meest gecommercialiseerde antimicrobiële nanodeeltjes en is verwerkt in consumentenproducten, van producten voor persoonlijke verzorging, zoals zeep en tandpasta, tot wasmachines en koelkasten, zelfs kinderproducten, zoals in kindersokken om geurtjes te voorkomen.
Onderzoekers van het iThree Institute van UTS bestudeerden nanozilver-adaptatiefenomenen in de bacterie Pseudomonas aeruginosa, in zijn biofilmvorm van groei, en observeerden een nieuw adaptatiemechanisme dat niet werd gezien in eerdere planktonische groeistudies. Na langdurige behandeling doodde nanozilver 99,99% van de bacteriepopulatie, waarbij slechts 0,01% cellen langer overleefden. Deze minieme fractie van ‘persisters’ hervatte de normale groei na stopzetting van de behandeling met nanodeeltjes.
“Begrijpen hoe ziekteverwekkers aanpassingsmechanismen aan nanodeeltjes ontwikkelen, is essentieel in onze inspanningen om de verschijnselen te overwinnen, ook in biofilms als de belangrijkste vorm van groei van pathogene bacteriën. Dit is om de werkzaamheid van belangrijke alternatieve antimicrobiële stoffen, zoals nanozilver, te beschermen in dit tijdperk van toenemende antibioticaresistentie,” zei hoofdauteur Dr. Cindy Gunawan.
De eerste auteur van het onderzoek, Dr. Riti Mann, zei dat de onderzoeksresultaten ook zullen helpen bij het ontwikkelen van strategieën voor een beter beheer van het gebruik van nanodeeltjes als antimicrobiële middelen, met name die met langdurige blootstelling.
“Op basis van deze studie raden we aan om patiënten niet alleen tijdens, maar ook na langdurig gebruik van nanodeeltjesbehandeling te monitoren voor bescherming tegen terugkerende infecties.
“Het wetenschappelijke bewijs dat bacteriën zich kunnen aanpassen aan nanodeeltjes, betekent dat we effectieve regulering van het gebruik van nanodeeltjes nodig hebben, met duidelijke risico’s versus voordelen en duidelijke antimicrobiële doelen. Met de beperkte ontwikkeling van nieuwe effectieve antibiotica in de afgelopen decennia, moeten we de werkzaamheid behouden van de alternatieve antimicrobiële middelen om onbehandelbare infecties te bestrijden, waardoor levens en miljarden dollars in de gezondheidszorg worden gered”, zei Dr. Gunawan.
De bacterie die in het onderzoek werd gebruikt, Pseudomonas aeruginosa, hecht zich vaak aan katheteroppervlakken, maar ook aan wonden en longvoeringen, waardoor biofilms groeien, die moeilijk te beheersen kunnen zijn.
Riti Mann et al, Evolutie van biofilmvormende pathogene bacteriën in aanwezigheid van nanodeeltjes en antibiotica: aanpassingsverschijnselen en kruisresistentie, Tijdschrift voor nanobiotechnologie (2021). DOI: 10.1186/s12951-021-01027-8
Geleverd door University of Technology, Sydney