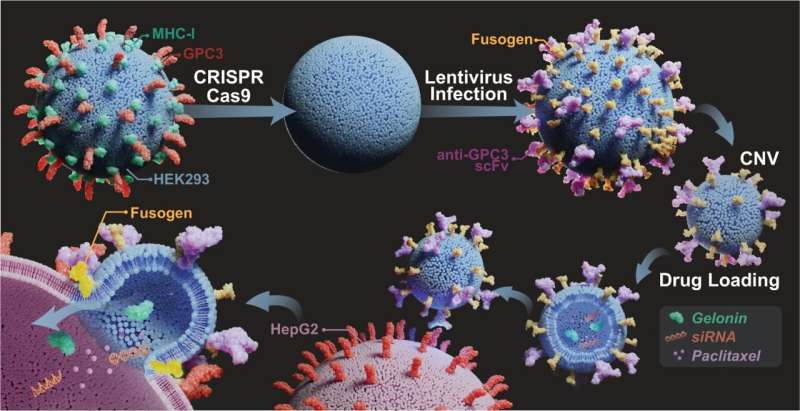
Schema van anti-GPC3-spot en gemanipuleerd fusogeen dat eFT-CNV’s tot co-expressie brengt voor cytosolische toediening van therapieën. Intrinsieke GPC3 en B2M worden uitgeschakeld met behulp van CRISPR/Cas 9, gevolgd door co-expressie van anti-GPC3 scFv en gemanipuleerd fusogeen op HEK293-celmembranen. De eFT-CNV’s worden gegenereerd door mechanische extrusie van de donorcellen en geladen met verschillende medicijnen, bijvoorbeeld nucleïnezuren, eiwittoxines of chemotherapeutische middelen, voor cytosolische toediening op het doelwit. Credit: Natuurcommunicatie (2023). DOI: 10.1038/s41467-023-39181-2
Twee ongelukkige feiten over chemotherapie: het kan zowel gezonde als kankercellen beschadigen, en veel therapeutische doelen blijven binnen kankercellen, waardoor ze moeilijker te bereiken zijn.
Biomedische ingenieurs van de Binghamton University behoren tot degenen die onderzoek doen naar het gebruik van van cellen afgeleide nanovesicles om therapeutische middelen met een grotere nauwkeurigheid en efficiëntie in het inwendige van kankercellen te brengen. De kleine zakjes eiwitten, lipiden en RNA die cellen afscheiden als een methode van intercellulaire communicatie, kunnen worden aangepast om medicijnen te vervoeren.
“Deze nanodragers hebben een aantal uitstekende eigenschappen”, zegt Yuan Wan, een assistent-professor aan het Thomas J. Watson College of Engineering and Applied Science’s Department of Biomedical Engineering. “Ze kunnen bijvoorbeeld worden geoogst uit menselijke celstammen, dus de immuunrespons is erg laag. Dat zorgt voor optimale biocompatibiliteit, zodat ze immuunklaring omzeilen en een verlengde bloedhalfwaardetijd hebben. De tijd voor circulatie door het lichaam is misschien 45 seconden, dus de met medicijnen beladen nanoblaasjes kunnen vele malen veilig naar de tumoren reizen en de medicijnen hebben meer kans om door kankercellen te worden opgenomen in vergelijking met medicijnen die vrijelijk in het lichaam worden geïntroduceerd.
“Grote hoeveelheden ingekapselde medicijnen kunnen goed worden beschermd en vastgehouden door de lipidemembranen van de nanovesicles. Zodra kankercellen deze nanovesicles opnemen, doden hoge medicijnconcentraties in de micro-omgeving van de tumor kankercellen effectief. Ter vergelijking: vrije medicijnen kunnen snel diffunderen en vervolgens uit het lichaam worden verwijderd. Slechts een zeer kleine hoeveelheid medicijnen bereikt de tumoren, waardoor de effectiviteit van de behandeling erg laag is. Je kunt de dosis verhogen, maar een hogere dosis resulteert ook in hoge systematische toxiciteit. ”
In hun nieuwe studie, gepubliceerd in Natuurcommunicatieexperimenteerde het Binghamton-team met het richten van delen en ontwikkelde virale fusogenen, dit zijn eiwitten die het richten op kanker en de fusie van celmembranen vergemakkelijken.
Door het identificeren van tot overexpressie gebrachte of kankerspecifieke antigenen die voorkomen in kwaadaardige cellen en het gebruik van doeldelen en met fusogen uitgeruste nanoblaasjes, worden ingekapselde geneesmiddelen in kankercellen geïnjecteerd terwijl gezonde cellen met rust worden gelaten.
“Mensen gebruiken op grote schaal nanodragers die bekend staan als met polymeer versierde liposomen, en ze zijn al goedgekeurd door de FDA, ” zei Wan. “Maar ze zijn niet perfect, omdat ze geen enkel kankergericht effect hebben en zeer ernstige immunogeniciteitsproblemen kunnen hebben [triggering a response by the immune system].”
In 2021 deed Wan onderzoek om van plasma afgeleide extracellulaire blaasjes te testen om vast te stellen of solitaire longknobbeltjes die in menselijke longen worden aangetroffen, goedaardig of kwaadaardig zijn. Andere methoden om maligniteit vast te stellen, duren te lang of zijn invasiever.
Door gebruik te maken van die kennis, maakt dit huidige maar afzonderlijke onderzoek gebruik van nanoblaasjes zodat ze voor ons werken en specifiek zijn in wat ze beïnvloeden. Idealiter zouden artsen deze doeldelen en met fusogen co-uitgeruste nanoblaasjes kunnen voorbereiden voor gebruik bij veiligere vaccinafgifte en genetische manipulatie.
Wat de toekomst betreft, zei Wan: “We moeten hun behandelingseffectiviteit aantonen in grote diermodellen en aantonen dat we geen grote hoeveelheid van deze blaasjes nodig hebben omdat we de membraanfusiefunctie hebben. Als je het aantal blaasjes en medicijnen die je nodig hebt, verlaagt u de kosten van de behandeling en de bijwerkingen. ”
Meer informatie:
Lixue Wang et al, Bio-geïnspireerde engineering van fusogen en nanovesicles die zijn uitgerust met delen, Natuurcommunicatie (2023). DOI: 10.1038/s41467-023-39181-2
Tijdschrift informatie:
Natuurcommunicatie
Aangeboden door de Binghamton-universiteit