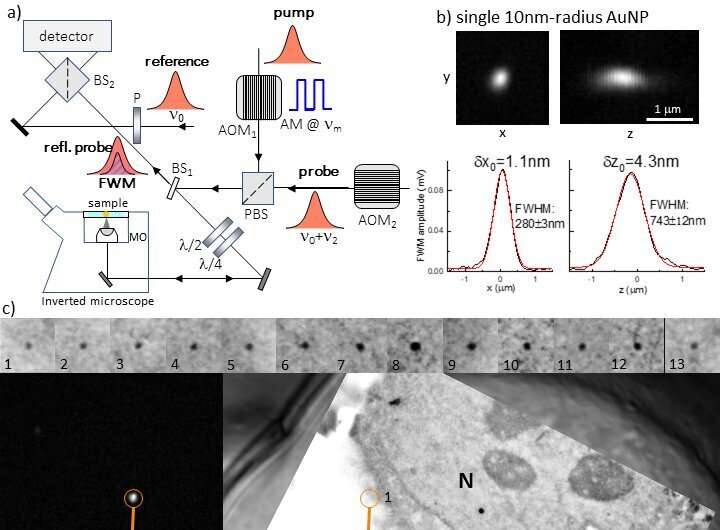
a) Schets van FWM-opstelling. Korte optische pulsen in resonantie met de optische absorptiepiek van een gouden nanodeeltje (AuNP) worden met behulp van een omgekeerde microscoop op het monster gefocusseerd en genereren een FWM-veld dat wordt verzameld in epi-geometrie, gedetecteerd met een heterodyne interferentieschema. AOM: akoestisch-optische modulator. (P)BS: (polariserende) bundelsplitser. P: polarisator. MO: microscoopobjectief. b) Voorbeeld van volumetrische FWM-microscopie op een enkele AuNP met een straal van 10 nm, met lijnprofielen langs x en z op de y-positie in het midden van de AuNP en overeenkomstige Gaussiaanse passingen (rode lijnen). De nauwkeurigheid van de zwaartepuntlokalisatie op nanoschaal in 3D (δx0=1,1 nm, δz0=4,3 nm) en de volledige breedte op half maximum (FWHM) verkregen uit de aanpassing worden aangegeven. c) CLEM van AuNP’s met een straal van 10 nm gebonden aan het epidermale groeifactoreiwit in menselijke kankercellen (HeLa). Individuele AuNP’s worden zonder achtergrond gedetecteerd in FWM (links), direct gemeten op 300 nm dikke harssecties na celfixatie, klaar voor EM-analyse. Hetzelfde patroon wordt gevonden in transmissie EM (TEM), gemarkeerd door de oranje cirkels. Twee cellen zijn zichtbaar, met hun kern aangegeven (N). De kern is omgeven door het organelbevattende cytoplasma. De bovenste rij toont gewassen (0,2 μm × 0,2 μm) van het TEM-beeld voor elke AuNP zoals genummerd. Het confocale reflectiebeeld dat gelijktijdig met FWM is verkregen, wordt onder het TEM-beeld weergegeven. Grijsschalen lopen van 0 tot M zoals aangegeven (M=1 komt overeen met 31 mV rms gedetecteerd). Credits: Iestyn Pope, Hugh Tanner, Francesco Masia, Lukas Payne, Kenton Paul Arkill, Judith Mantell, Wolfgang Langbein, Paola Borri en Paul Verkade
Correlatieve lichtelektronenmicroscopie (CLEM) is een krachtig hulpmiddel bij bioimaging, omdat het de mogelijkheid combineert om levende cellen over grote gezichtsvelden af te beelden met moleculaire specificiteit met behulp van lichtmicroscopie (LM) met de hoge ruimtelijke resolutie en ultrastructurele informatie van elektronenmicroscopie (EM ). Om interessante biomoleculen te markeren en hun positie met hoge nauwkeurigheid in CLEM te bepalen, moeten onderzoekers ervoor zorgen dat ze worden gelabeld met sondes die zowel zichtbaar zijn in LM (meestal door fluorescentie) als in EM (met behulp van elektronendicht materiaal). Bestaande sondes hebben echter een aantal nadelen, waaronder een gebrek aan stabiliteit onder LM (fotobleken) en een gebrek aan integriteit.
In een nieuw artikel gepubliceerd in Lichtwetenschap & toepassingheeft een team van wetenschappers onder leiding van professor Paola Borri van Cardiff University en professor Paul Verkade van de University of Bristol, Verenigd Koninkrijk, een nieuwe CLEM-benadering ontwikkeld die kleine gouden nanodeeltjes gebruikt als een enkele sonde die zichtbaar is in zowel LM als EM met hoge contrast en fotostabiliteit, zonder dat er fluorescerende sondes nodig zijn.
Voor LM maakten ze gebruik van een optische microscoop die was ontwikkeld in de groep van professor Borri. Deze microscoop detecteert de niet-lineaire optische respons van gouden nanodeeltjes, genaamd four-wave mixing (FWM). Met deze methode waren de onderzoekers in staat om individuele kleine gouden nanodeeltjes te detecteren als enkele sondes van het epidermale groeifactor-eiwit in menselijke kankercellen, gelokaliseerd met nanometrische precisie zonder achtergrond door lichtmicroscopie, en correlatief in kaart gebracht met hoge nauwkeurigheid naar het overeenkomstige transmissie-elektron. microscopie beeld.
Dankzij de achtergrondvrije en fotostabiele FWM-respons van individuele gouden nanodeeltjes, goed zichtbaar in EM vanwege hun elektronendichte samenstelling, opent FWM-CLEM nieuwe wegen voor zeer nauwkeurige correlatieve microscopie-workflows zonder de noodzaak om onstabiele fluoroforen of aanvullende vaste merkers te gebruiken, waardoor de protocollen voor monstervoorbereiding aanzienlijk worden vereenvoudigd.
De wetenschappers vatten het werkingsprincipe van hun FWM-microscoop als volgt samen: “In zijn algemene vorm is FWM een niet-lineair licht-materie-interactieverschijnsel van de derde orde waarbij drie lichtvelden in een medium interageren om een vierde golf te genereren. Hier hebben we een schema gebruiken waarbij alle lichtgolven dezelfde middenfrequentie hebben, in resonantie met de optische absorptiepiek van een gouden nanodeeltje. Voor excitatie en detectie gebruiken we een combinatie van korte optische pulsen van ongeveer 150 fs duur, pomp en sonde genaamd, gegenereerd door De gedetecteerde FWM kan worden opgevat als een door een pomp veroorzaakte verandering in het vermogen van het gouden nanodeeltje om licht door te laten en te verstrooien, wat zich manifesteert als een verandering in de sondestraal die door het deeltje wordt verstrooid in aanwezigheid van de pomp.
“FWM-detectie is opmerkelijk fotostabiel en hoog contrast. Met deze methode zijn we in staat om individuele kleine (tot een straal van 5 nm) gouden nanodeeltjes te detecteren in verstrooiende en automatisch fluorescerende cellen en weefsels, volledig vrij van achtergrond, met beeldsnelheden en excitatievermogens die compatibel zijn met live-celbeeldvorming, met een gevoeligheid die alleen wordt beperkt door fotonschotruis. We hebben ook gezien dat FWM een gevoelige verslaggever is van gouden nanodeeltjesvormen, veelbelovend voor multiplexing door vormherkenning in toekomstige toepassingen. ”
De onderzoekers concluderen: “FWM-CLEM opent nieuwe opwindende mogelijkheden voor correlatieve licht-elektronenmicroscopie-workflows, waarbij bestaande beperkingen worden overwonnen met fluorescerende sondes en/of vaste markeringen die niet nodig zijn in onze methode. Over het algemeen geloven we dat FWM-CLEM een wijdverspreide Gecombineerd met bestaande strategieën om bijvoorbeeld gouden nanodeeltjes in virionen te labelen of zelfs in te kapselen, opent FWM het opwindende vooruitzicht om enkele virionen gedurende lange observatietijden te volgen, zonder achtergrond en diep in levende cellen en weefsels, om ze vervolgens te lokaliseren gebeurtenissen van belang (bijv. genoomvrijgave) in de context van de cellulaire ultrastructuur door CLEM.”
Meer informatie:
Iestyn Pope et al, Correlatieve licht-elektronenmicroscopie met kleine gouden nanodeeltjes als enkele sondes, Licht: wetenschap en toepassingen (2023). DOI: 10.1038/s41377-023-01115-4
Tijdschrift informatie:
Licht: wetenschap en toepassingen
Aangeboden door de Chinese Academie van Wetenschappen