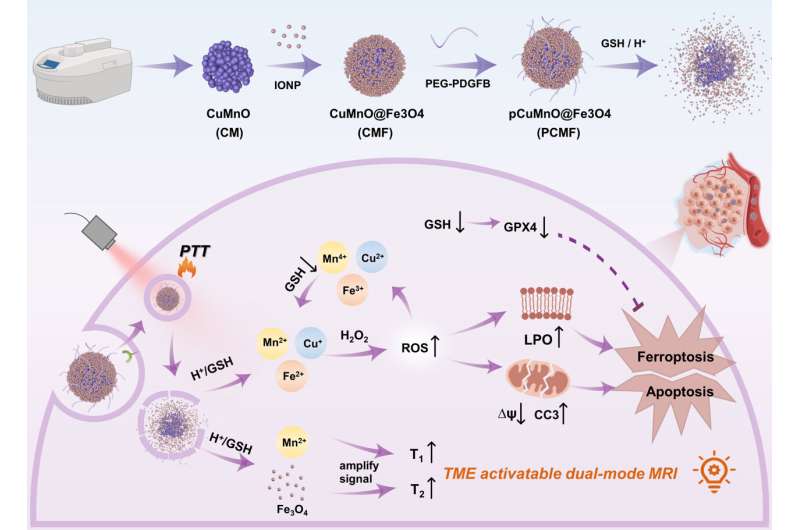
Schematische voorstelling. Krediet: Xie Wenteng
Onlangs heeft een onderzoeksteam onder leiding van prof. Wu Zhengyan van Hefei Institutes of Physical Science, Chinese Academy of Sciences, in samenwerking met de Binzhou Medical University, met succes een nanostructuur ontworpen die de detectie en behandeling van tumoren verbetert.
Hun werk, onlangs gepubliceerd in Kleinricht zich op het creëren van een zeer specifieke methode voor het diagnosticeren en behandelen van tumoren met behulp van een combinatie van magnetische resonantiebeeldvorming en enzymactiviteit.
“Bepaalde chemische reacties, de metaalion-gemedieerde Fenton-achtige reactie genoemd, kunnen snel de niveaus van schadelijke reactieve zuurstofsoorten verhogen en de tumorgroei vertragen,” zei prof. Wu, “en enzymen gemaakt van koper, die een hoge katalytische activiteit hebben en goed reageren op de tumoromgeving, zijn niet erg stabiel.”
Daarom maakt de ontwikkeling van een core-shell nano-theranostisch middel dat reageert op de micro-omgeving van tumoren een vroege tumordiagnose en monitoring van de effectiviteit van de behandeling mogelijk en worden op koper gebaseerde nano-enzymen beschermd tegen deactivering als gevolg van sterische hinder.
Om dit probleem aan te pakken, ontwikkelde het onderzoeksteam een gespecialiseerd nano-enzym genaamd CuMnO@Fe3O4 (CMF) met een kern-schilstructuur die reageert op de micro-omgeving van de tumor. Vervolgens bevestigden ze PDGFB-richtliganden aan het oppervlak van CMF, waardoor een specifiek nano-enzym voor tumoren ontstond dat bekend staat als PCMF.
Het kern-omhulselontwerp van PCMF voorkomt interferentie van thiolgroepen die in grote moleculen worden aangetroffen tijdens de circulatie in de bloedbaan. Dit bevordert de antitumoractiviteit van PCMF.
PCMF vertoont zowel T1- als T2-beeldvormingsmogelijkheden met dubbel contrast wanneer geactiveerd door zwak zuur en glutathion. Dit betekent dat het een verbeterd beeldcontrast kan bieden voor het diagnosticeren van tumoren.
Bovendien wordt PCMF afgebroken in de micro-omgeving van de tumor, waarbij zowel metaalionen als ultraklein ijzeroxide vrijkomen. Dit proces verbruikt glutathion, versnelt Fenton- en Fenton-achtige reacties, verhoogt het niveau van intracellulaire reactieve zuurstofsoorten en induceert apoptose en ferroptose in kankercellen.
PCMF bezit ook het vermogen tot fotothermische conversie en kan dus worden gebruikt voor gecombineerde fotothermische en nanokatalytische therapie, waardoor de antikankeractiviteit wordt versterkt.
Volgens het team biedt dit werk inzicht in het bereiken van een zeer gevoelige tumorspecifieke therapeutische diagnose.
Meer informatie:
Wenteng Xie et al., Tumormicro-omgeving-geactiveerde nanostructuur om MRI-mogelijkheden en nanozyme-activiteit te verbeteren voor zeer tumorspecifieke multimodale theranostiek, Klein (2023). DOI: 10.1002/klein.202306446
Tijdschriftinformatie:
Klein
Geleverd door de Chinese Academie van Wetenschappen