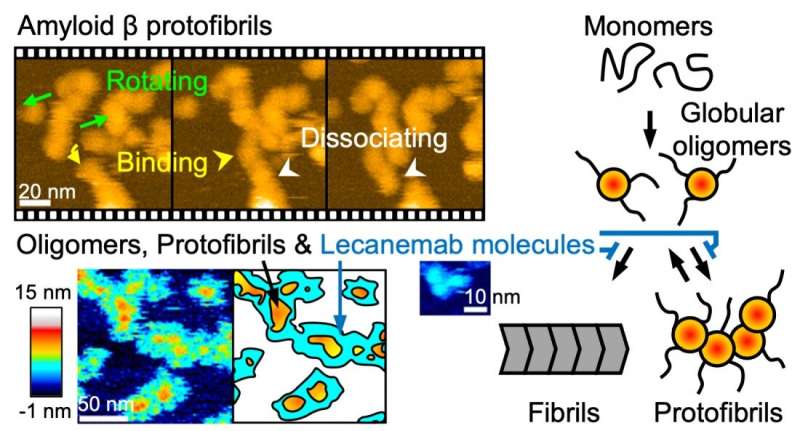
High-speed atomic force microscopie en schematische visualisatie van protofibrillen – dynamiek, binding, dissociatie en biochemische interacties. Krediet: American Chemical Society
Dat melden onderzoekers van Kanazawa University Nano-brieven hoe snelle atoomkrachtmicroscopie leidt tot inzichten in processen die relevant zijn voor de ziekte van Alzheimer. Bovendien blijkt de techniek een uitstekend hulpmiddel te zijn om het effect van medicijnen tegen de ziekte te bestuderen.
Volgens de amyloïdehypothese wordt de ziekte van Alzheimer, de meest voorkomende vorm van dementie, veroorzaakt door gebreken in de productie, accumulatie en verwijdering van amyloïde-bèta (Aβ) in de hersenen. Aβ verwijst naar een groep peptiden (eiwitfragmenten) die na verloop van tijd plaques vormen in de hersenen van mensen met de ziekte van Alzheimer. Er zijn geneesmiddelen ontwikkeld die erop gericht zijn de aggregatie van Aβ te verminderen, maar recente bevindingen tonen aan dat verschillende soorten Aβ-aggregaten een verschillende bijdrage leveren aan de ontwikkeling van de ziekte van Alzheimer.
Met name intermediaire aggregaten zoals protofibrillen zijn giftiger dan de eigenlijke uiteindelijke fibrillen, het hoofdbestanddeel van Aβ-plaques. Een nauwkeurig begrip van de complexe aggregatieroutes is daarom noodzakelijk voor de verdere ontwikkeling van efficiënte geneesmiddelen tegen de ziekte van Alzheimer. Kenjiro Ono van Kanazawa University en collega’s zijn er nu in geslaagd om de structurele dynamiek van protofibrillen te visualiseren, evenals het effect van een recent ontwikkeld medicijn op basis van anti-Aβ-antilichamen.
De wetenschappers keken met behulp van high-speed atomic force microscopy (HS-AFM) naar de vorming en de structuur van Aβ-protofibrillen. De laatste methode is de afgelopen jaren naar voren gekomen als een krachtig hulpmiddel voor nanoimaging voor het bestuderen van biomoleculen en hun dynamiek met een hoge spatiotemporele resolutie. HS-AFM-waarnemingen toonden aan dat protofibrillen een knoopstructuur hebben, met stabiele structurele kenmerken – met name de bindingshoek tussen knopen – over verschillende monsters. Belangrijk is dat deze knoopstructuur verschilt van echte, volwassen fibrillen, die een spiraalvormige structuur hebben.
Ono en collega’s onderzochten vervolgens de dissociatie van protofibrillen. Ze ontdekten dat de lengte van protofibrillen afhangt van hun concentratie, wat suggereert dat aggregaten spontaan kunnen dissociëren.
Om gedetailleerd inzicht te krijgen in de werking van anti-Aβ-antilichaamgeneesmiddelen, onderzochten de onderzoekers de binding tussen Aβ-protofibrillen en een nieuw medicijn dat bekend staat als lecanemab. Ze ontdekten dat het bindingsvermogen (affiniteit) van lecanemab voor protofibrillen vrijwel onafhankelijk is van de grootte van de protofibrillen – met andere woorden, de affiniteit varieert niet substantieel tijdens het aggregatieproces. HS-AFM-waarnemingen onthulden verder dat lecanemab het oppervlak van kleine pre-protofibril-aggregaten bedekt. Daarbij remt het medicijn de verdere aggregatie tot protofibrillen, wat op zijn beurt de vorming van echte Aβ-fibrillen en plaques voorkomt.
De resultaten van Ono en collega’s leveren direct bewijs van een mechanisme waardoor een antilichaammedicijn het Aβ-aggregatieproces verstoort. Meer in het algemeen bevestigt het werk de veelzijdigheid van de HS-AFM-methode voor het bestuderen van biochemische routes. “Single-molecule HS-AFM is een effectief hulpmiddel om de structurele dynamiek van voorbijgaande, metastabiele amyloïde-aggregatie-tussenproducten en de effecten van anti-aggregerende medicijnen daarop te onthullen”, aldus de onderzoekers.
High-speed atoomkrachtmicroscopie
Het algemene principe van atoomkrachtmicroscopie (AFM) is om met een zeer kleine tip het oppervlak van een monster te scannen. Tijdens deze horizontale (xy) scan volgt de tip, die aan een kleine cantilever is bevestigd, het verticale (z) profiel van het monster, waardoor een kracht op de cantilever wordt opgewekt die kan worden gemeten. De grootte van de kracht op de xy-positie kan worden gerelateerd aan de z-waarde; de xyz-gegevens die tijdens een scan worden gegenereerd, resulteren vervolgens in een hoogtekaart met structurele informatie over het onderzochte monster. Bij high-speed-AFM (HS-AFM) is het werkingsprincipe iets meer betrokken: de cantilever wordt gemaakt om te oscilleren in de buurt van zijn resonantiefrequentie. Wanneer de tip over een oppervlak wordt bewogen, worden de variaties in de amplitude (of de frequentie) van de oscillatie van de cantilever – als gevolg van de interactie van de tip met het oppervlak van het monster – geregistreerd, aangezien deze een maat vormen voor de lokale “z” -waarde.
HS-AFM resulteert in een video, waarbij het tijdsinterval tussen de frames afhangt van de snelheid waarmee een enkel beeld kan worden gegenereerd (door het sample xy-scannen). Onderzoekers van Kanazawa University hebben de afgelopen jaren HS-AFM verder ontwikkeld, zodat het kan worden toegepast om biochemische moleculen en biomoleculaire processen real-time te bestuderen. Kenjiro Ono en collega’s hebben de methode nu toegepast om de structurele dynamiek van amyloïde-bèta-protofibrillen te bestuderen, waarvan bekend is dat ze een cruciale rol spelen in de pathogenese van de ziekte van Alzheimer, evenals het effect van een anti-amyloïde-bèta-antilichaamgeneesmiddel tegen de ziekte. .
Meer informatie:
Takahiro Watanabe-Nakayama et al, Structurele dynamiek van amyloïde-β-protofibrillen en acties van anti-amyloïde-β-antilichamen zoals waargenomen door snelle atoomkrachtmicroscopie, Nano-brieven (2023). DOI: 10.1021/acs.nanolett.3c00187
Tijdschrift informatie:
Nano-brieven
Aangeboden door de Kanazawa-universiteit