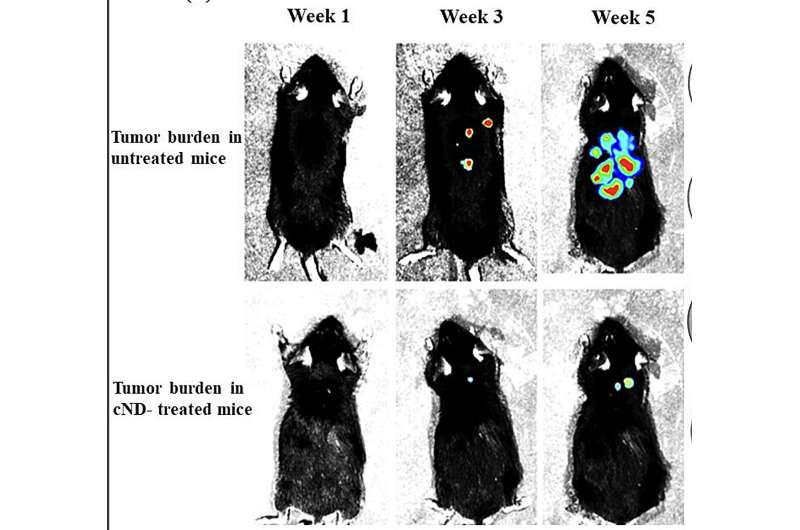
Effect van behandeling met koolstofnanodiamanten op de groei en metastase van B16F10-Luc2-tumor bij muizen door bioluminescentiebeeldvorming. Krediet: Behera et al
Nanodiamanten zijn koolstofnanodeeltjes van 2–8 nm, die gemakkelijk kunnen worden gefunctionaliseerd met verschillende chemische groepen zoals carboxylgroepen of medicijnen. Eerder onderzoek heeft aangetoond dat actief delende cellen een grotere kans hebben om nanodiamanten te absorberen en dat epitheelcellen die zijn behandeld met carbonzuurnanodiamanten het vermogen verliezen om door celdoorlaatbare cellulosemembranen te migreren.
Rajiv K. Saxena en collega’s onderzochten of nanodiamanten de uitzaaiing van tumoren zouden kunnen blokkeren, een proces dat celmigratie naar nieuwe gebieden vereist. Het onderzoek is gepubliceerd in het journaal PNAS-nexus.
De auteurs behandelden B16F10-melanoomcellen met carbonzuurnanodiamanten in kweek en testten hun vermogen om te migreren en binnen te dringen door polycarbonaatmembranen met poriën van 8 µm. De auteurs ontdekten dat de nanodiamanten het vermogen van melanoomcellen om te migreren blokkeerden, terwijl onbehandelde tumorcellen het membraan konden passeren.
Muizen (C57Bl/6) die B16F10-melanoomtumorcellen toegediend kregen en vervolgens behandeld werden met carbonzuurnanodiamanten vertoonden weinig of geen uitzaaiingen van tumoren, terwijl onbehandelde muizen hun tumoren zagen groeien en zich naar nieuwe delen van het lichaam verplaatsten.
De overleving van de tumordragende muizen behandeld met carbonzuurnanodiamanten was ook significant beter dan onbehandelde tumordragende muizen.
Gebaseerd op bewijs van genexpressie, veronderstellen de auteurs dat de kleine koolstofnanodiamanten het losbreken van kankercellen uit de primaire tumormassa kunnen remmen – en daaropvolgende stappen van metastase kunnen blokkeren, zoals de fysieke beweging van cellen en hun vermogen om bloedvaten binnen te dringen. .
Volgens de auteurs moeten nanodiamanten verder worden onderzocht als mogelijk therapeutisch middel voor de uitzaaiing van kanker.
Meer informatie:
Sushreesangita P. Behera et al., Carboxyl-nanodiamanten remmen melanoomtumormetastasen door de cellulaire motiliteit en invasiviteit te blokkeren, PNAS-nexus (2023). DOI: 10.1093/pnasnexus/pgad359
Tijdschriftinformatie:
PNAS-nexus
Geleverd door PNAS Nexus