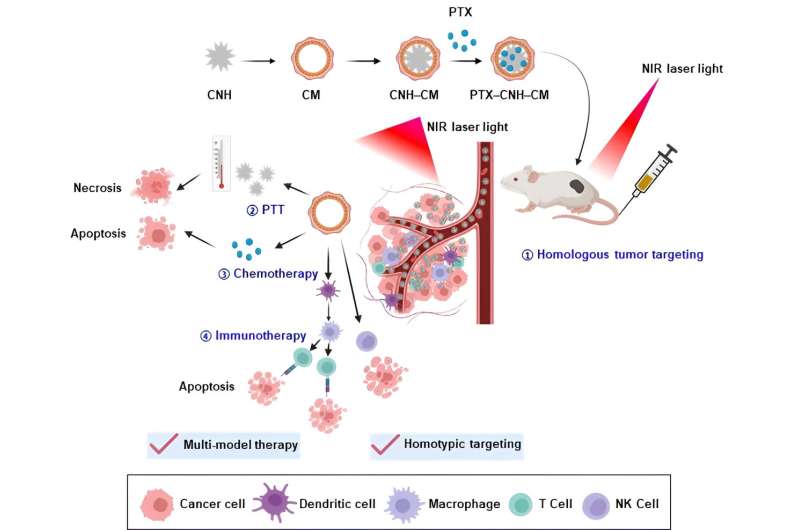
Biomimetische koolstof nanohorn complexen voor de behandeling van kanker. Onderzoekers ontwikkelen een nieuw biomimetisch koolstof nanohorn complex met kankercelmembranen en paclitaxel voor efficiënte toediening van medicijnen aan de beoogde plaats. Deze aanpak integreert fotothermische therapie, chemotherapie en immunotherapie om kanker en metastatische ziekten te bestrijden. Credit: Eijiro Miyako van JAIST
Kanker blijft een van de meest uitdagende ziekten om te behandelen vanwege de complexiteit en de neiging om te metastaseren (verspreiden naar, of binnendringen in, nabijgelegen weefsels of verre plekken in het lichaam om nieuwe tumoren te vormen). Traditionele therapieën, zoals chemotherapie en bestraling, hebben vaak beperkingen zoals niet-specifieke targeting en ernstige bijwerkingen.
Als reactie hierop wenden onderzoekers zich tot innovatieve benaderingen die meerdere therapeutische modaliteiten combineren om deze problemen aan te pakken. Deze studie onderzoekt een geavanceerde oplossing met CNH’s om een multimodaal fototheranostisch platform voor kanker te creëren dat fotothermische therapie (PTT), immunotherapie en chemotherapie integreert.
PTT maakt gebruik van lichtgevoelige materialen die een fotothermisch effect kunnen veroorzaken [conversion of near-infrared (NIR) light to heat] en immuunreacties activeren om kankercellen te vernietigen. Hoewel PTT effectief is bij het aanpakken van solide tumoren, heeft het aanzienlijke beperkingen.
Een groot nadeel is het onvermogen om kankercellen buiten het bestralingsgebied te elimineren, waardoor het minder effectief is tegen metastatische ziekten. Bovendien wordt de werkzaamheid van PTT beperkt door de diepte van de NIR-lichtpenetratie, wat het vermogen om diepgewortelde tumoren te behandelen kan belemmeren.
Om deze beperkingen aan te pakken, heeft een team van onderzoekers onder leiding van universitair hoofddocent Eijiro Miyako van het Japan Advanced Institute of Science and Technology (JAIST) nu CNH-nanodeeltjes ontwikkeld die zijn omwikkeld met kankercelmembranen (CM’s) voor de toediening van paclitaxel (PTX) voor de behandeling van darmkanker.
Deze nanodeeltjes maken gebruik van de unieke eigenschappen van CNH’s en de targetingmogelijkheden van kankercelmembranen. Door kankermembranen te gebruiken, kunnen de nanodeeltjes specifiek kankercellen targeten, waardoor de precisie van PTT wordt verbeterd.
Hun onderzoek bevindingen werden gepubliceerd in Kleine wetenschap.
Om de therapeutische uitkomsten verder te verbeteren, hebben onderzoekers het chemotherapeutische of antikankermedicijn PTX ingekapseld in de CNH‒CM-complexen. Deze nanodeeltjes zijn niet alleen ontworpen om therapeutische middelen rechtstreeks aan tumoren af te leveren, maar ook om de werkzaamheid van het medicijn te maximaliseren. Ze hebben deze nanodeeltjes getest op tumortargeting, medicijnafgifte en therapeutische effecten in experimentele modellen.
De onderzoekers ontdekten dat de PTX-CNH‒CM-complexen een hoge accumulatie en langdurige retentie op de tumorlocatie vertoonden. Dit resulteerde in een sterker chemotherapeutisch effect vergeleken met vrije PTX. Bovendien vertoonden de nanodeeltjes een robuust fotothermisch effect en significante immuunreacties, waardoor tumoren effectief werden vernietigd.
“Het grote oppervlak en de unieke eigenschappen van CNH verbeteren de medicijnbelading en de fotothermische conversie-efficiëntie. Bovendien maakt CM gerichte toediening mogelijk, terwijl de ingekapselde PTX en immunotherapeutische eigenschappen van de drager extra therapeutische voordelen bieden. Zo resulteerde de integratie van PTT, immunotherapie en chemotherapie binnen één platform in synergetische effecten, waardoor de beperkingen van standalone PTT werden overwonnen,” legt Dr. Miyako uit.
De biomimetische CNH-nanocomplexen vertoonden uitstekende tumor-targeting, gecontroleerd medicijn-afgevend gedrag en inductie van kankerceldood, wat leidde tot een sterke antitumorrespons. Deze bevindingen suggereren dat het biomimetische CNH-complexsysteem een veelbelovende weg vertegenwoordigt voor de ontwikkeling van nauwkeurigere en effectievere kankerbehandelingen, wat een significante vooruitgang in kankertherapie markeert.
“Onze studie biedt een effectieve en nauwkeurige aanpak voor de behandeling van kanker en metastatische ziekten door de voordelen van meerdere therapeutische modaliteiten te combineren in één platform. We verwachten dat deze technologie binnen 10 jaar beschikbaar zal zijn voor klinische proeven”, concludeert Dr. Miyako.
Meer informatie:
Nina Sang et al, Biomimetische functionele nanocomplexen voor fotothermische kanker chemoimmunotheranostics, Kleine wetenschap (2024). DOI-bestand: 10.1002/smsc.202400324
Aangeboden door Japan Advanced Institute of Science and Technology