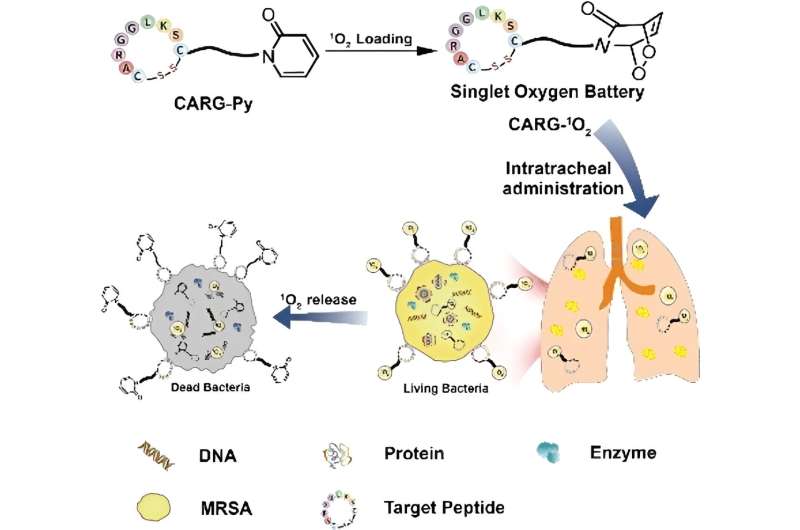
Credit: Angewandte Chemie International Edition (2023). DOI: 10.1002/anie.202306803
Bij antibacteriële fotodynamische therapie wordt bestraling gebruikt om reactieve zuurstofsoorten te produceren die bacteriën doden. Omdat er extern licht en zuurstof nodig is, is deze methode alleen geschikt voor oppervlakkige infecties.
In het journaal Angewandte Chemieheeft een Chinees onderzoeksteam nu een moleculaire “singlet zuurstofbatterij” geïntroduceerd die kan worden “opgeladen” met reactieve zuurstof, die vervolgens wordt vrijgegeven in diepe weefsellagen om zich te richten op methicilline-resistente stafylokokken.
Antibioticaresistente bacteriën zijn in opmars. Hoewel ze vaak onschadelijk zijn voor gezonde mensen, gebruiken gevreesde multiresistente ‘ziekenhuispathogenen’ zoals methicilline-resistente Staphylococcus aureus (MRSA) verwondingen of verse chirurgische wonden om toegang te krijgen tot het lichaam. Ze infecteren ook immuungecompromitteerde patiënten. Omdat antibiotica niet effectief zijn, is er soms geen remedie.
Een veelbelovend alternatief is antibacteriële fotodynamische therapie, die al veel wordt gebruikt in de tandheelkunde. Bij deze techniek wordt een door licht geactiveerde stof (photosensitizer) bestraald, die een fotodynamische reactie op gang brengt die singletzuurstof produceert (1O2), een opgewonden vorm van zuurstof.
In tegenstelling tot antibiotica valt deze stof tegelijkertijd meerdere biomoleculaire locaties op de bacterie aan. Het is gemakkelijk te gebruiken, veilig, pijnloos en over het algemeen vrij van bijwerkingen. Helaas is het alleen nuttig geweest voor oppervlakte-infecties, omdat het noodzakelijke licht maar enkele millimeters in het weefsel doordringt. Bovendien hebben diepere weefsellagen ook niet genoeg zuurstof voor een effectieve behandeling.
Een team onder leiding van Bingran Yu en Fu-Jian Xu aan de Beijing University of Chemical Technology heeft nu een nieuwe benadering van fotodynamische therapie ontwikkeld: een “singlet zuurstofbatterij” die kan worden gebruikt om diepe bacteriële infecties te bestrijden omdat er geen licht of externe zuurstof voor nodig is .
De omzetting van zuurstof in reactieve singlet-zuurstof door bestraling in aanwezigheid van een molecuul dat licht opvangt (photosensitizer) vindt als eerste plaats. De “batterij” wordt “opgeladen” met de singlet-zuurstof. Deze “batterij” bestaat uit een speciale stikstofhoudende, zesledige ring van koolstofatomen (pyridon) die de singlet-zuurstof stevig bindt.
Het reactieve zuurstofmolecuul overbrugt twee tegenovergestelde hoekpunten van de ring (endoperoxide). Een aan de ring gebonden peptide “herkent” specifiek MRSA-bacteriën, zodat de moleculaire batterijen zich rond en in de bacteriën ophopen en continu hun singlet-zuurstof afgeven.
De bacteriën worden dus tegelijkertijd op veel verschillende locaties aangevallen, inclusief hun membraan, DNA, enzymen en andere eiwitten. Dit maakt het ontwikkelen van resistentie vrijwel onmogelijk. Bij toediening aan muizen door middel van verneveling bleek de singlet-zuurstofbatterij zeer effectief te zijn bij de behandeling van longinfecties veroorzaakt door MRSA. Systemische bijwerkingen werden niet waargenomen.
Meer informatie:
Yiwen Zhu et al, A Targeting Singlet Oxygen Battery for Multidrug-Resistant Bacterial Deep-Tissue Infections, Angewandte Chemie International Edition (2023). DOI: 10.1002/anie.202306803
Tijdschrift informatie:
Angewandte Chemie International Edition
,
Angewandte Chemie
Aangeboden door Wiley