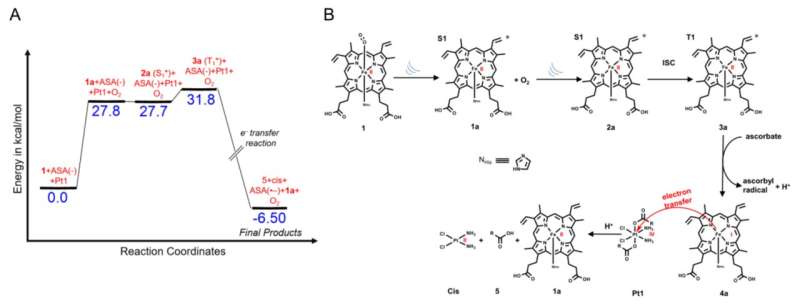
Voorgesteld mechanisme van de vermindering van de PtIV prodrug Pt1 met de penta-gecoördineerde sonosensitizer met behulp van DFT-berekeningen. (A) Energieprofieldiagram van de reductie, wat aangeeft dat de reactie thermodynamisch ongunstig is. (B) Voorgesteld reductiemechanisme . Credit: Angewandte Chemie International Edition (2023). DOI: 10.1002/anie.202301074
Chemotherapiebehandelingen produceren sterke bijwerkingen. Een nieuw agens dat zich ophoopt in het tumorweefsel en daar door ultrasone golven wordt geactiveerd, heeft dit probleem niet.
Platinacomplexen behoren tot de meest gebruikte medicijnen tegen kanker. Ze zijn succesvol, maar hebben ernstige bijwerkingen. Een internationaal onderzoeksteam onder leiding van Dr. Johannes Karges van de Faculteit Scheikunde en Biochemie van de Ruhr Universiteit in Bochum, Duitsland, heeft een complex ontwikkeld dat zich ophoopt in tumorweefsel en daar wordt geactiveerd door ultrasone golven.
Het celbeschadigende effect ontvouwt zich dus alleen daar waar het eigenlijk gewenst is. “Waar eerdere studies vertrouwden op lichtactiveringen die slechts enkele millimeters diep in het weefsel kunnen doordringen, hebben we nu een behandelmethode ontwikkeld met ultrasone activering die enkele centimeters diep in het lichaam doordringt”, zegt Karges.
Dit zou een behandeling met weinig bijwerkingen mogelijk kunnen maken, zelfs voor grote en diepgewortelde tumoren. De onderzoekers publiceerden hun resultaten in Angewandte Chemie International Edition.
Onschadelijk in gezond weefsel
De platina(II)-complexen cisplatine, oxaliplatine en carboplatine behoren tot de meest gebruikte geneesmiddelen tegen kanker. Hun klinische succes wordt tenietgedaan door ernstige bijwerkingen, zoals misselijkheid, braken, nierbeschadiging en beenmergsuppressie. Om deze beperkingen te overwinnen, zijn de afgelopen decennia grote onderzoeksinspanningen geïnvesteerd in de ontwikkeling van zogenaamde platina(IV)-complex-prodrugs.
“Deze prodrugs zijn stabiel en inactief, dus ze zijn volkomen onschadelijk”, legt Johannes Karges uit. “In gezond weefsel zouden ze zo moeten blijven. In kankerweefsel zouden ze echter snel moeten worden omgezet in de therapeutisch actieve platina(II)-complexen.”
Voor de reductie van het metaalcomplex is energie nodig. Eerdere studies meldden activatie met ultraviolet, blauw of rood licht. “Het probleem is dat licht slechts minder dan een centimeter diep in het lichaam kan doordringen en dus niet veel tumoren bereikt”, legt Johannes Karges uit. Om deze beperking te overwinnen, heeft zijn team voor het eerst platina(IV)-complex-prodrugs gecombineerd met sonosensitizers die selectief kunnen worden geactiveerd met ultrasone bestraling.
Nanodeeltjes hopen zich op in de tumor
Om een therapeutisch effectief complex te ontwikkelen, kapselden de onderzoekers de prodrugs van het platina(IV)-complex en de sonosensitizers samen in hemoglobine in om nanodeeltjes te vormen. “We konden waarnemen dat de nanodeeltjes zich selectief ophoopten in een darmtumor van een muis na injectie in de bloedbaan, waardoor een gerichte behandeling werd ondersteund”, meldt Johannes Karges.
“Na bestraling met ultrageluid werd de platina(IV)-prodrug geactiveerd op de plaats van de tumor, waardoor cisplatine vrijkwam, dat toxisch is voor cellen, en de tumor bijna volledig werd uitgeroeid.”
Voordelen van echografie
Deze resultaten kunnen de weg vrijmaken voor de ontwikkeling van nieuwe technieken en middelen voor de behandeling van zeer grote of diepgewortelde tumoren. Echografie kan meer dan een orde van grootte dieper in het weefsel doordringen dan nabij-infrarood licht. Bovendien worden ultrasone behandelingen over het algemeen als minder invasief en gebruiksvriendelijk beschouwd. Een ander voordeel is dat ziekenhuizen meestal al zijn uitgerust met de benodigde apparatuur. “Ons werk is nog steeds fundamenteel onderzoek”, benadrukt Johannes Karges.
“Of en wanneer behandelingen op basis hiervan in de klinische praktijk kunnen worden aangeboden, is nog niet te overzien.”
Meer informatie:
Ganghao Liang et al., Vermindering van platina(IV)-prodrug hemoglobine-nanodeeltjes met diep doordringende ultrageluidstraling voor tumorgerichte therapeutisch verbeterde antikankertherapie, Angewandte Chemie International Edition (2023). DOI: 10.1002/anie.202301074
Tijdschrift informatie:
Angewandte Chemie International Edition
Aangeboden door Ruhr-Universitaet-Bochum