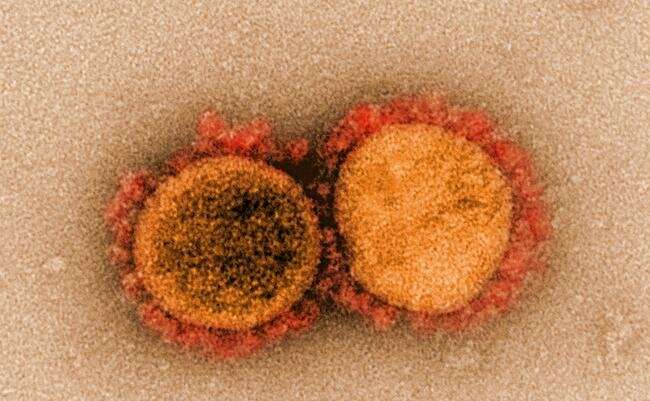
Transmissie-elektronenmicrofoto van SARS-CoV-2-virusdeeltjes, geïsoleerd van een patiënt. Beeld vastgelegd en in kleur verbeterd bij de NIAID Integrated Research Facility (IRF) in Fort Detrick, Maryland. Krediet: NIAID
Wetenschappers volgen een nieuwe strategie in de langdurige strijd tegen het SARS-CoV-2-virus door nanobodies te ontwikkelen die virusvarianten op twee verschillende manieren kunnen neutraliseren.
In laboratoriumstudies identificeerden onderzoekers twee groepen moleculen die effectief waren tegen virusvarianten. Met behulp van verschillende mechanismen omzeilden nanobodies in elke groep mutaties en maakten ze het virus onmogelijk om zich te binden aan de receptor waardoor het gastheercellen kon binnendringen.
Hoewel vaccinatie de hervatting van sommige pre-pandemische activiteiten in delen van de wereld mogelijk maakt, werkt SARS-CoV-2 snel om vaccins heen door zichzelf te muteren. In deze studie neutraliseerden de nanobodies drie opkomende varianten: Alpha, Beta en Gamma.
“Bedrijven zijn al begonnen met het introduceren van de zorgwekkende varianten in de constructie van boostershots van de bestaande vaccins”, zegt Kai Xu, assistent-professor veterinaire biowetenschappen aan de Ohio State University en mede-hoofdauteur van het onderzoek. “Maar het virus muteert voortdurend en de snelheid van mutatie is misschien sneller dan we kunnen vastleggen. Daarom moeten we meerdere mechanismen gebruiken om de verspreiding van het virus te beheersen.”
Een versnelde artikelvoorbeeld van de studie wordt online gepubliceerd in Natuur.
Nanobodies zijn antilichamen die zijn afgeleid van de immunisatie van kameelachtige zoogdieren – zoals kamelen, lama’s en alpaca’s – die opnieuw kunnen worden ontworpen tot kleine moleculen die de structuren en functies van menselijke antilichamen nabootsen.
Voor dit werk hebben de onderzoekers lama’s geïmmuniseerd om enkelketenige antilichamen tegen SARS-CoV-2 te produceren. Ze immuniseerden ook “nanomice”, transgene muizen met een kameelachtigen-gen dat was ontwikkeld door onderzoekscollega Jianliang Xu in het laboratorium van Rafael Casellas, senior onderzoeker bij het National Institute of Arthritis and Musculoskeletal and Skin Diseases (NIAMS), om nanobodies te genereren die vergelijkbaar zijn met tot die geproduceerd door kameelachtigen.
Het team versterkte de kracht van de nanobodies door de dieren eerst te immuniseren met het receptorbindingsdomein (RBD), een deel van het virale oppervlakte-spike-eiwit, en vervolgens met boostershots die het volledige spike-eiwit bevatten.
“Door deze sequentiële immunisatiestrategie te gebruiken, hebben we nanobodies gegenereerd die het virion kunnen vangen door het receptorbindende domein met zeer hoge affiniteit te herkennen,” zei Xu.
De wetenschappers testten de neutralisatiecapaciteit van verschillende nanobodies, brachten het oppervlak van het RBD in kaart, voerden functionele en structuuranalyses uit en meten de sterkte van hun affiniteit om de kandidaat-moleculen van een grote bibliotheek tot zes te verkleinen.
Het coronavirus is zeer besmettelijk omdat het zich zeer hecht aan de ACE2-receptor bindt om toegang te krijgen tot long- en neusholtecellen bij mensen, waar het kopieën van zichzelf maakt om andere cellen te infecteren. Het receptorbindende domein op het spike-eiwit is van fundamenteel belang voor het succes ervan bij het hechten aan ACE2.
“Die RBD-ACE2-interface bevindt zich bovenaan het receptorbindende domein – dat gebied is het primaire doelwit voor de beschermende menselijke antilichamen, gegenereerd door vaccinatie of eerdere infectie, om de virale toegang te blokkeren,” zei Xu. “Maar het is ook een regio die vaak gemuteerd is in de varianten.”
De manier waarop mutanten tot nu toe zijn ontstaan, suggereert dat langdurige afhankelijkheid van de huidige vaccins uiteindelijk in gevaar zal komen, zeggen de onderzoekers, omdat de effectiviteit van antilichamen aanzienlijk wordt beïnvloed door die mutanten op het grensvlak.
“We ontdekten dat bepaalde nanobodies een geconserveerd gebied van het receptorbindende domein kunnen herkennen, een verborgen locatie die te smal is voor menselijke antilichamen om te bereiken,” zei Xu. En door op deze locatie te bevestigen, ook al is het op enige afstand van waar RBD verbinding maakt met ACE2, wordt nog steeds bereikt wat de bedoeling is: het blokkeren van SARS-CoV-2 om een gastheercel binnen te gaan.
De andere groep nanobodies, aangetrokken door de RBD-ACE2-interface, terwijl ze in hun oorspronkelijke vorm bepaalde varianten niet konden neutraliseren. Toen de onderzoekers deze groep echter construeerden als homotrimeren – drie exemplaren die in tandem zijn gekoppeld – bereikten de nanobodies een krachtige neutralisatie van het virus. Het op dezelfde manier veranderen van de structuur van de nanobodies die aan het geconserveerde gebied van RBD waren gehecht, verhoogde ook hun effectiviteit.
Er is nog veel meer onderzoek in het verschiet, maar de bevindingen suggereren dat nanobodies veelbelovende instrumenten kunnen zijn om COVID-19-sterfte te voorkomen wanneer vaccins worden aangetast, zei Xu.
“Ons toekomstplan is om antilichamen specifiek tegen opkomende varianten voor therapeutische ontwikkeling verder te isoleren en een betere oplossing voor vaccins te vinden door van die antilichamen te leren,” zei hij.
Jianliang Xu et al, Nanobodies van kameelachtige muizen en lama’s neutraliseren SARS-CoV-2-varianten, Natuur (2021). DOI: 10.1038/s41586-021-03676-z
Natuur
Geleverd door de Ohio State University