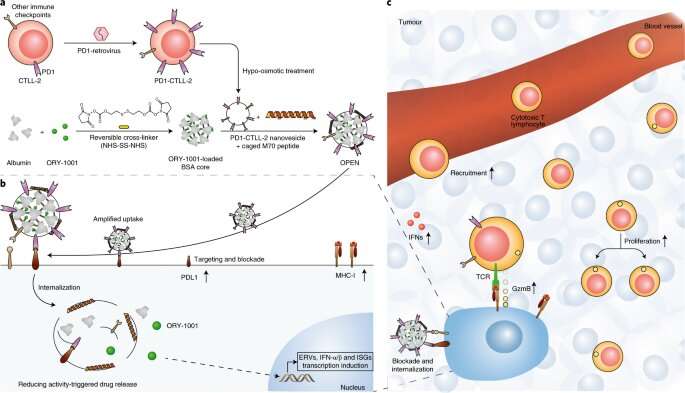
Fig. 1: Schematische weergave van de voorbereiding en het werkingsmechanisme van OPEN. Krediet: DOI: 10.1038/s41565-021-00972-7
Immunotherapie tegen kanker, zoals immuuncheckpointblokkade (ICB) is een revolutionaire behandeling tegen tumoren door de immuunsurveillance te versterken en zelfs ziektebestrijding op de lange termijn te induceren.
Type I-interferonen (IFN’s) zijn de belangrijkste coördinatoren van de interactie tussen tumoren en het immuunsysteem. Verslechterde IFN-signalering wordt geassocieerd met een slechte prognose bij patiënten met colonkanker, melanoom, triple-negatieve borstkanker, enz. De huidige aanvullende IFN-therapie brengt soms ernstige bijwerkingen en IFN-geïnduceerd multigene resistentieprogramma met zich mee voor ICB.
In een studie gepubliceerd in Natuur Nanotechnologie, toonde een onderzoeksteam onder leiding van Li Yaping en Zhang Pengcheng van het Shanghai Institute of Materia Medica van de Chinese Academie van Wetenschappen (CAS) aan dat de paradoxale effecten van aanvullende IFN-therapie kunnen worden aangepakt met behulp van een met T-lymfocytmembraan versierde epigenetische nano-inductor van IFN’s ( OPEN).
De onderzoekers hebben eerst een geprogrammeerde doodsreceptor 1 (PD1) tot overexpressie brengende cytotoxische T-cellijn genetisch gemanipuleerd en vervolgens het membraan van deze cellen gebruikt om eiwitnanodeeltjes te omhullen die zijn geladen met ORY-1001, een remmer van lysine-specifieke histondemethylase 1 (LSD1) , om OPEN te maken.
Ze onthulden dat de OPEN de intratumorale accumulatie van ORY-1001 en de lokale productie van IFN’s na intraveneuze toediening verbeterde, en toonden aan dat de IFN’s de tumorinfiltratie, proliferatie en activiteit van tumorspecifieke cytotoxische T-cellen en antigeenweergave van tumorcellen verhoogden.
Bovendien bewezen ze dat het door IFN geïnduceerde geprogrammeerde doodsligand 1 (PDL1) en andere immuuncheckpoint-moleculen gemakkelijk werden geneutraliseerd door daaropvolgende OPEN. Dit sequentiële proces vulde specifiek intratumorale IFN’s aan en verlichtte door IFN geïnduceerde immuunontduiking, en dus vertraagde tumorgroei in meerdere tumormodellen.
“De studie demonstreert een elegante strategie om de paradoxale effecten van aanvullende IFN-therapie op te lossen met behulp van epigenetische nano-inducer van IFN’s. Het is een mijlpaal op het gebied van nanogeneeskunde voor veiligere en effectievere immunotherapie bij kanker”, zegt prof. Zhao Yuliang, een academicus van CAS .
“Dit is het eerste onderzoek dat het grote potentieel van epigenetische nanogeneeskunde in kankerimmunotherapie uitwerkt. De nanogeneeskunde heeft een significante klinische translatiewaarde vanwege de voordelen in tumorgerichte levering en immuuncontrolepuntblokkade”, zei prof. Hao Xishan, een academicus van de Chinese Academie van Ingenieurswetenschappen (CAE).
Yihui Zhai et al, T-lymfocytmembraan versierde epigenetische nano-inductor van interferonen voor immunotherapie van kanker, Natuur Nanotechnologie (2021). DOI: 10.1038/s41565-021-00972-7
Natuur Nanotechnologie
Geleverd door de Chinese Academie van Wetenschappen