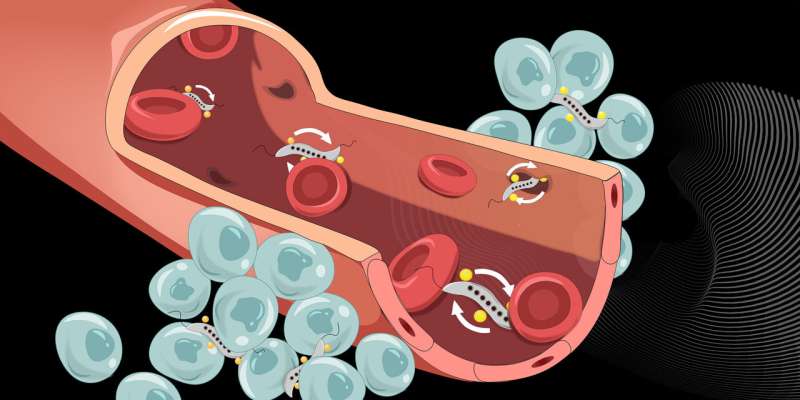
Magnetische bacteriën (grijs) kunnen door nauwe intercellulaire ruimten dringen om de bloedvatwand te passeren en tumoren te infiltreren. Krediet: Yimo Yan / ETH Zürich
Wetenschappers over de hele wereld onderzoeken hoe geneesmiddelen tegen kanker het meest efficiënt de tumoren kunnen bereiken waarop ze zich richten. Een mogelijkheid is om gemodificeerde bacteriën te gebruiken als “veerboten” om de medicijnen door de bloedbaan naar de tumoren te vervoeren. Onderzoekers van ETH Zürich zijn er nu in geslaagd bepaalde bacteriën onder controle te houden, zodat ze effectief de bloedvatwand kunnen passeren en tumorweefsel kunnen infiltreren.
Onder leiding van Simone Schürle, hoogleraar Responsive Biomedical Systems, kozen de onderzoekers van ETH Zürich ervoor om te werken met bacteriën die van nature magnetisch zijn vanwege de ijzeroxidedeeltjes die ze bevatten. Deze bacteriën van het geslacht Magnetospirillum reageren op magnetische velden en kunnen worden gecontroleerd door magneten van buiten het lichaam.
Tijdelijke hiaten benutten
In celculturen en bij muizen hebben Schürle en haar team nu aangetoond dat een roterend magnetisch veld dat op de tumor wordt toegepast, het vermogen van de bacteriën om de vaatwand in de buurt van de kankergroei te passeren, verbetert. Bij de vaatwand stuwt het roterende magnetische veld de bacteriën voort in een cirkelvormige beweging.
Om beter te begrijpen hoe het mechanisme om de vaatwand te passeren werkt, is een gedetailleerde blik nodig: de bloedvatwand bestaat uit een laag cellen en dient als een barrière tussen de bloedbaan en het tumorweefsel, dat door vele kleine bloedvaten wordt doordrongen . Smalle ruimtes tussen deze cellen laten bepaalde moleculen uit de vaatwand door. Hoe groot deze intercellulaire ruimten zijn, wordt geregeld door de cellen van de vaatwand, en ze kunnen tijdelijk breed genoeg worden om zelfs bacteriën door de vaatwand te laten gaan.
Sterke voortstuwing en hoge waarschijnlijkheid
Met behulp van experimenten en computersimulaties konden de onderzoekers van ETH Zürich aantonen dat het voortstuwen van de bacteriën met behulp van een roterend magnetisch veld om drie redenen effectief is. Ten eerste is voortstuwing via een roterend magnetisch veld tien keer krachtiger dan voortstuwing via een statisch magnetisch veld. Deze laatste geeft slechts de richting aan en de bacteriën moeten op eigen kracht bewegen.
De tweede en meest kritieke reden is dat bacteriën die worden aangedreven door het roterende magnetische veld constant in beweging zijn en zich langs de vaatwand voortbewegen. Hierdoor is de kans groter dat ze de openingen tegenkomen die zich kort tussen vaatwandcellen openen in vergelijking met andere voortstuwingstypen, waarbij de beweging van de bacterie minder verkennend is. En ten derde, in tegenstelling tot andere methoden, hoeven de bacteriën niet te worden gevolgd via beeldvorming. Zodra het magnetische veld over de tumor is gepositioneerd, hoeft het niet opnieuw te worden aangepast.
‘Cargo’ hoopt zich op in tumorweefsel
“We maken ook gebruik van de natuurlijke en autonome voortbeweging van de bacterie”, legt Schürle uit. “Als de bacteriën eenmaal door de bloedvatwand zijn gegaan en zich in de tumor bevinden, kunnen ze zelfstandig diep in het binnenste migreren.” Om deze reden gebruiken de wetenschappers de voortstuwing via het externe magnetische veld slechts een uur lang genoeg voor de bacteriën om efficiënt door de vaatwand te gaan en de tumor te bereiken.
Dergelijke bacteriën zouden in de toekomst geneesmiddelen tegen kanker kunnen dragen. In hun celkweekstudies simuleerden de onderzoekers van ETH Zürich deze toepassing door liposomen (nanosferen van vetachtige stoffen) aan de bacteriën te hechten. Ze labelden deze liposomen met een fluorescerende kleurstof, waardoor ze in de petrischaal konden aantonen dat de bacteriën inderdaad hun “lading” in het kankerweefsel hadden afgeleverd, waar het zich ophoopte. In een toekomstige medische toepassing zouden de liposomen worden gevuld met een medicijn.
Bacteriële kankertherapie
Bacteriën gebruiken als veerboten voor medicijnen is een van de twee manieren waarop bacteriën kunnen helpen in de strijd tegen kanker. De andere benadering is meer dan honderd jaar oud en beleeft momenteel een opleving: gebruik maken van de natuurlijke neiging van bepaalde soorten bacteriën om tumorcellen te beschadigen. Hierbij kunnen verschillende mechanismen betrokken zijn. Het is in ieder geval bekend dat de bacteriën bepaalde cellen van het immuunsysteem stimuleren, die vervolgens de tumor elimineren.
Meerdere onderzoeksprojecten onderzoeken momenteel de werkzaamheid van het gebruik van E. coli-bacteriën tegen tumoren. Tegenwoordig is het mogelijk om bacteriën te modificeren met behulp van synthetische biologie om hun therapeutische effect te optimaliseren, bijwerkingen te verminderen en ze veiliger te maken.
Niet-magnetische bacteriën magnetisch maken
Maar om de inherente eigenschappen van bacteriën in kankertherapie te gebruiken, blijft de vraag hoe deze bacteriën de tumor efficiënt kunnen bereiken. Hoewel het mogelijk is om de bacteriën direct in tumoren nabij het oppervlak van het lichaam te injecteren, is dit niet mogelijk voor tumoren diep in het lichaam. Dat is waar de microrobotbesturing van professor Schürle om de hoek komt kijken. “We geloven dat we onze technische benadering kunnen gebruiken om de effectiviteit van bacteriële kankertherapie te vergroten”, zegt ze.
E. coli die in de kankeronderzoeken wordt gebruikt, is niet magnetisch en kan dus niet worden voortgestuwd en gecontroleerd door een magnetisch veld. Over het algemeen is magnetische respons een zeer zeldzaam fenomeen bij bacteriën. Magnetospirillum is een van de weinige geslachten van bacteriën die deze eigenschap hebben.
Schürle wil daarom ook E. coli-bacteriën magnetisch maken. Dit zou het ooit mogelijk kunnen maken om een magnetisch veld te gebruiken om klinisch gebruikte therapeutische bacteriën te bestrijden die geen natuurlijk magnetisme hebben.
T. Gwisai et al, Magnetische, door koppel aangedreven levende microrobots voor verhoogde tumorinfiltratie, Wetenschap Robotica (2022). DOI: 10.1126/scirobotics.abo0665. www.science.org/doi/10.1126/scirobotics.abo0665
Wetenschap Robotica
Aangeboden door ETH Zürich